MONUMENTI E INQUINAMENTO
L'inquinamento atmosferico e i monumenti
"L'Italia è l'unico paese al mondo in cui la storia ha sempre coinciso con la creazione di opere d'arte, sia di pittura che di scultura e di architettura civile, religiosa o funeraria" (1). Tale patrimonio caratterizza tutte le regioni della penisola, dalle Alpi alla Sicilia, interessando non solo le grandi città, le "capitali dell'arte" famose in tutto il mondo, ma anche numerosi piccoli centri che conservano testimonianze significative del passato, a dimostrazione di un tessuto storico-artistico largamente diffuso sul territorio.
Tali opere, soprattutto quelle all'aperto nei centri urbani, sono spesso sottoposte all'azione dell'inquinamento atmosferico che, come minaccia le condizioni di salute degli esseri umani, così deturpa l'aspetto e deteriora, a volte irrimediabilmente, lo stato di conservazione dei monumenti, provocando vistosi annerimenti, formazioni di croste nere, sgretolamenti ecc. Si considera inquinante atmosferico qualsiasi sostanza, artificiale o naturale, gassosa o particellare, che sia estranea alla composizione naturale dell'atmosfera o che la alteri. "Generalmente l'inquinante è presente in piccole quantità ed è tuttavia capace di provocare effetti misurabili sugli esseri viventi o sui materiali in quanto la sua azione si protrae nel tempo con processi di accumulo"(2).
Tra le iniziative volte a studiare le conseguenze dell'inquinamento atmosferico sui monumenti, un posto importante spetta al simposio tenutosi a Roma dal 15 al 17 ottobre 1986, organizzato dall'Istituto per la Conservazione dell'Università di Goteborg e intitolato "Air Pollution and Conservation, Safeguarding Our Architectural Heritage". In quell'occasione vennero presentati i risultati dell'attività svolta da gruppi di lavoro operanti in diverse città europee per rilevare l'impatto dell'inquinamento sul patrimonio culturale, e si definirono anche metodologie e approcci specialistici al problema. Da questa iniziativa internazionale trasse origine il volume, significativamente intitolato "Città inquinata I monumenti", curato da Italia Nostra e pubblicato nel 1989 (3). Esso contiene, oltre a saggi sull'argomento e a proposte di linee d'intervento, un'indagine campione sugli effetti dell'inquinamento su venti facciate di edifici romani e analoghe indagini condotte da gruppi di ricerca nazionali nelle città di Ankara, Atene, Colonia, Cracovia e Goteborg. Un aspetto innovativo di tale lavoro fu la collaborazione di studiosi di discipline diverse (storici dell'arte, architetti, urbanisti, chimici, fisici, biologi, restauratori, economisti ecc.), come poi è diventato frequente in molti odierni interventi di restauro.
L'inquinamento non è un fenomeno nuovo, del tempo presente, ma ha una lunga storia, a partire dall'epoca classica in cui scrittori come Teofrasto e Seneca già ne fecero menzione, come è ricordato da Peter Brimblecombe (Scuola di Scienze ambientali. Università dell'East Anglia Norwich, Regno Unito) in un saggio dedicato all'inquinamento atmosferico nel passato (4). Una testimonianza in età moderna del fenomeno è contenuta in una relazione del 1785 in cui "...i Provveditori del Sal, magistrati della Repubblica Veneta, vennero messi in allarme per l'inquinamento dell'aria con i gas ammoniacali e l'ossido di carbonio diffuso dalle vetrerie di Murano e dal riscaldamento casalingo, perché nocivo alle pitture"(5). Diverse sono poi le testimonianze riguardanti la città di Londra, dove gli effetti dell'inquinamento sono documentati a partire dal XIII-XIV secolo ed in modo particolare dal XIX secolo, in concomitanza con la rivoluzione industriale.
La novità della situazione attuale, quindi, non consiste tanto nella natura del fenomeno, quanto nel fatto che i processi di deterioramento dei materiali, avvenuti, per quanto riguarda l'Italia, in tempi lenti e controllabili fino alla metà circa del XIX secolo, hanno poi subito un'accelerazione allarmante per gravità ed estensione. Tutti i materiali che costituiscono i monumenti all'aperto ne sono più o meno colpiti: pietre porose come i calcari e le arenarie e più compatte come il travertino e il marmo, intonaci, laterizi e persino metalli. è difficile stabilire i tempi di degrado per ogni singolo materiale, perché sono molte le variabili coinvolte nel processo; inoltre, da uno studio di Giorgio Torraca (Università di Roma, Facoltà di Ingegneria) risulta anche che "la velocità di degrado di un dato materiale in un dato ambiente dipende dai danni che esso ha subito nel corso della sua storia precedente; microfratture causate da tensionamenti meccanici e sali formati da processi chimici costituiscono una "memoria" che il materiale conserva dell'attacco ambientale. Questa "memoria" si accumula progressivamente e rende il materiale sempre più suscettibile agli attacchi successivi"(6).
Si approfondiscono, in particolare, le cause di degrado della pietra, la cui superficie è spesso soggetta ad annerimenti, formazione di croste nere, fratture, sgretolamenti, con cadute più o meno consistenti di materiale lapideo.
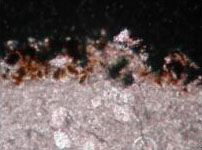
Cause del degrado della pietra
Tutte le pietre presentano un fenomeno di degradazione naturale sotto l'aspetto fisico e chimico, e in climi non estremi come i nostri gli effetti del deterioramento derivano da una mescolanza delle due azioni. Inoltre si deve ricordare che le rocce hanno composizioni chimiche diverse che le rendono più o meno predisposte a subire un'alterazione, soprattutto a seconda del tipo di grana interna di cui si compongono (7).Le precipitazioni sono spesso responsabili di diversi tipi di alterazione delle rocce. Le rocce carbonatiche in genere (marmi), essendo ricche di argille illitiche, sono poco solubili, ma in particolari condizioni, in presenza cioè di anidride carbonica e di acqua, presentano un fenomeno di trasformazione della loro composizione chimica a bicarbonati solubili (con PH decisamente basici), secondo la reazione sottostante. (Un esempio di tale trasformazione sono i fenomeni carsici)
CaCO3 + CO2+H2O ‹-› Ca(HCO3)2
Calcite (carbonato di calcio) poco solubile ‹-› Bicarbonato di calcio solubile
Calcite (carbonato di calcio) poco solubile ‹-› Bicarbonato di calcio solubile
Come si può notare dalla reazione, il fenomeno è pure reversibile, in quanto, per eliminazione di acqua e di CO2, si può tornare alla formazione di carbonato di calcio.
Un altro fenomeno naturale che interessa la parte argillosa delle pietre calcaree è quello di idrolisi dei silicati, ossia un'alterazione legata alla cattura di ioni H+ presenti in acque leggermente acide da parte dei silicati. Le argille illitiche presentano struttura chimica di base a tre strati T-O-T ( legame fra due strutture tetraedriche, T, con una ottaedrica composta da cationi, O), con alte percentuali di silicati e alluminio, intervallata da cationi come Na+, K+, Ca+,Mg+ e molecole di acqua. Con precisione, la formula delle argille illitiche può essere schematizzata come segue:
KxAl4(OH)4Si8-XAlXO20 . H2O (con x < 2 generalmente 1<x<1,5)
Gli ioni H+ si pongono all'interno di tale struttura spostandovi gli altri cationi, portandoli in soluzione. Tale fenomeno è influenzato dal clima, dalla composizione stessa della roccia, dalla temperatura, dalla quantità di precipitazioni, dal PH dell'acqua meteorica.
I solidi cristallini, inoltre, hanno la caratteristica peculiare dell'anisotropia, ossia tendono a modificare le loro proprietà fisiche a secondo della direzione di sollecitazioni o dilatazioni.
Una sollecitazione verticale potrà deformare il reticolo, comportando lo slittamento, l'uno sull'altro, dei piani reticolari diversi, formato da atomi tutti della stessa specie. Una sollecitazione obliqua, invece, implica lo slittamento di piani reticolari identici, formati però tutti da atomi di specie diverse e la resistenza alla deformazione si presenterà più debole, con il conseguente distacco tra i cristalli. Nel caso di aumenti di temperatura, la struttura iniziale e regolare della pietra, con distanze interatomiche e dalle proprietà meccaniche stabilite, collasserà pian piano, andando ad allentare la rigidità dell'edificio cristallino e a dilatarsi.
Un fenomeno che va ad interessare negativamente i rapporti intergranulari o intercristallini con conseguente scagliatura e frammentazione della roccia è l'infiltrazione d'acqua, soprattutto in climi molto freddi e acquosi o molto caldi.
Nel primo caso si verifica un fenomeno di gelo e di disgelo: l'acqua piovana, andando ad infilarsi all'interno degli spazi pi� profondi della roccia o nelle crepe formatesi, all'abbassarsi delle temperature gela, e dato che fisicamente tale fenomeno prevede un aumento di volume di circa il 9%, i capillari della pietra subiranno delle pressioni interne e successive variazione degli spazi intermolecolari, secondo ben determinati assi in rapporto al tipo di pressione. Un fenomeno simile può accadere quando l'acqua rimane imprigionata nella pietra dalla formazione di ghiaccio esternamente: quest'ultimo esercita delle spinte sull'acqua, che a sua volta comprime le pareti dei capillari rocciosi in cui è contenuta. Quando tali pressioni superano un certo limite, provocano la formazione di microcrepe che a lungo andare possono determinare vere e proprie fratture nella pietra.
Questo fenomeno è forse più frequente di quanto si possa immaginare, soprattutto in climi cosi facilmente variabili come i nostri, dove gelate, repentini innalzamenti di temperatura e successivi bruschi abbassamenti si alternano facilmente. Si formerà così del ghiaccio che si scioglierà per l'innalzamento della temperatura la quale, abbassandosi nuovamente, darà luogo alla solidificazione dalla superficie verso l'interno.
Nel caso, invece, di clima molto caldo, l'aumento di temperatura può causare una naturale dilatazione che quindi crea spazi intermolecolari e tensioni interne più deboli, causa di un ulteriore deterioramento.
La presenza di agenti naturali come fenomeni tettonici può essere causa di crepe e successivo insediamento di acque con i problemi sopra descritti in caso di gelo e di disgelo.
L'acqua, poi, essendo ricca di sali come cloruri, solfati, nitrati e nitriti, li deposita sulle superfici rocciose che, essendo porose, li trattengono al loro interno. Essendo sali solubili, si scioglieranno nuovamente con l'acqua, ma potranno ricristallizzare nelle porosità della pietra, soprattutto nei periodi caldi. L'evaporazione acquosa farà saturare la salinità delle acque meteoriche, dando luogo a quelle efflorescenze saline ben visibili sulle pietre. Facilmente tali sali potranno riprecipitare e ricristallizzare, in quanto la loro solubilità nell'acqua diminuirà fino alla saturazione della soluzione: i cristalli così prodotti si ingrosseranno, provocando le solite tensioni fra i capillari.
Le analisi fatte su pietre calcaree, come la pietra vicentina, hanno dimostrato la loro elevata porosità e addirittura una forte permeabilità all'acqua che, penetrando facilmente al loro interno, provoca i problemi sopra trattati.
Lo studio di pietre poste in atmosfere urbane ha mostrato come in tali pietre si intensifichi la seppur lenta, ma sempre presente azione naturale di degrado della pietra stessa.
In ambito urbano, tra le sostanze più pericolose per l'integrità delle pietre, ricordiamo gli ossidi di zolfo (SO2), di azoto (NOx), i residui di combustione di benzine, nafte e carboni (CO2), le polveri silicatiche e vari altri ossidi presenti nell'atmosfera. L'acqua svolge in questo caso una funzione fisica di trasporto e chimica tramite reazioni di solubilizzazione, facilitando, unita a queste sostanze, il fenomeno delle patine di alterazione e dei depositi nerastri che vanno sotto il nome di croste nere, forse i maggiori responsabili del degrado dei monumenti.
La presenza di zolfo nelle benzine e nafte crea durante la reazione di combustione la formazione di anidride solforosa (SO2), che a contatto con l'ossigeno atmosferico e con catalizzatori quali ferro o carbone si ossida ad anidride solforica (SO3) secondo la reazione:
SO2 + O2 —> SO3 + H2O
Questo composto, reagendo con l'acqua meteorica, crea un acido corrosivo:
SO3 + H2O —> H2SO4( la cosiddetta pioggia acida)
L'acido solforico reagisce con il marmo, il carbonato di calcio, e lo trasforma in gesso.
H2SO4 + CaSO4 + H2O —> CaSO4. 2 H2O + CO2
Si formano così dei microcristalli di gesso, noto per essere un materiale altamente poroso, che inglobano tutte le particelle solide contenute nella soluzione di partenza e soprattutto globuletti di carbone poroso derivati dalla combustione di oli minerali, ossidi di ferro e ferro o metalli pesanti presenti nelle vicinanze. È questa la cosiddetta crosta nera che si presenta sotto forma di microcristalli di gesso spesso tabulari, geminati, nelle tipiche disposizioni dette a "rosa del deserto".
Oltre al gesso, la presenza di ossidi di ferro, che creano la tipica colorazione scura della crosta, catalizzerà la reazione di ossidazione da SO2 a SO3, che, come già spiegato in precedenza, si lega all'acqua meteorica, creando acido solforico. Inizierà in tale modo il circolo vizioso di formazione delle croste nere e del loro ispessimento.
La crosta nera è un fenomeno che si ritrova negli interstizi e nelle zone più riparate dal dilavamento, dove può ispessirsi fino a divenire troppo pesante per autosostenersi, cadendo spontaneamente. Mette così a nudo porzioni di roccia sana in posizioni più profonde, che diventano terreno per la formazione di una nuova crosta nera. Si può quindi capire come tale processo porti ad un lento degrado della pietra stessa.
Un altro fenomeno di degrado è dovuto all'alta solubilità del gesso, che può così sciogliersi e venir dilavato, penetrando in soluzione dentro alle porosità di pietre tenere come la pietra di Vicenza, dove potrà ricristallizzare.
Una diversa forma di degrado della pietra, anch'essa importante, è il biodeterioramento derivato da processi biologici e microbiologici.
Qualsiasi organismo vivente, come alghe, muschi, licheni, piante superiori, ma anche insetti, volatili, mammiferi, può alterare permanentemente ed irreversibilmente la pietra. Questa azione può esplicarsi sia fisicamente che chimicamente. Nel primo caso può essere legata allo sviluppo dell'organismo all'interno dei pori e determinare una successiva frattura della pietra, accrescendo le tensioni destabilizzanti. Nel secondo caso è legata al metabolismo, alle deiezione animali, ricche di sostanze acide e saline che agiscono con un'azione rilevante di degrado chimico sulla roccia.
Tali fattori possono combinarsi, intensificando la loro azione di degrado soprattutto su rocce calcaree tenere.
Sono presenti poi organismi, i batteri chemiosintetici, che sono in grado di metabolizzare alcuni composti dello zolfo, dell'azoto e del ferro. Per esempio, i solfobatteri sono capaci di ridurre i solfiti e i solfati a solfuri e ossidare i solfuri ad acido solforico con le conseguenze già precedentemente citate.
Dalle analisi effettuate sulle croste nere risulta la presenza di tali batteri, ma perché questa fissazione di zolfo sulla pietra avvenga, necessita di grandi quantità di batteri sulle pietre e grandi concentrazioni di SO2 in atmosfera.
Deiezioni animali, quali guano di piccione, sono molto aggressive sulla pietra per la loro acidità e salinità, le quali provocano degradi chimici. Lo sfregamento delle unghie e del becco vanno invece ad incrementare le crepe preesistenti, danneggiando ulteriormente la superficie petrosa.
Infine, la pietra può presentarsi in condizioni precarie in conseguenza della lavorazione subita.
Il taglio o l'estrazione della pietra dalla cava provoca delle tensioni sulla sua struttura, e la lavorazione, se non viene attuata direttamente lungo i reticoli cristallini, può provocare rotture, microfratture, tensioni, luoghi di proliferazione di tutti quegli agenti già citati.
L'accostamento di materiali diversi, quali calcari teneri con metalli o altre superfici, anche colorate, può essere deleterio in quanto causa decolorazioni, ossidazioni e successive macchie dei calcari stessi che subiscono il dilavamento dei materiali con i quali sono a contatto.
NOTE
- M. VALSECCHI; Crisi del patrimonio artistico italiano, in AA. VV., La difesa del Patrimonio artistico, Milano, 1978, p. 9.
- M. MATTEINI A. MOLES, Scienza e restauro, Firenze, 1984, p. 280.
- AA. VV., Città inquinata i monumenti, a cura di a. Montanari e p. Petraroia, Roma, 1989.
- P. BRIMBLECOMBE, Per una ricostruzione dei fenomeni di inquinamento atmosferico nel passato, in AA. VV., Città inquinata, cit., pp. 2532.
- M. VALSECCHI, cit., p.23.
- G. TORRACA, Il volto della città, in AA. VV., Città inquinata, cit., p. 38.