LA QUALITÀ DELL'ARIA A MODENA
Lo smog e le sue origini
L'esempio d'inquinamento dell'aria più conosciuto in qualsiasi parte del mondo è certamente lo smog, presente soprattutto nelle grandi città. Ciò che produce questo smog, i reagenti, sono in gran parte le emissioni degli scarichi degli autoveicoli: tra tutte le attività dell'uomo l'uso dei veicoli a motore è in assoluto la più inquinante.La presenza di questo smog si identifica con una foschia di colore giallo-bruno, causata dalla sospensione, nell'aria, di piccole gocce d'acqua contenenti i prodotti delle reazioni chimiche avvenute tra gli inquinanti. Chi vive in una città di medio-grandi dimensioni troverà familiare questa descrizione, ma è anche vero che lo smog si diffonde rapidamente anche ad aree fino ad oggi incontaminate, come parchi naturali e altre zone scarsamente civilizzate.

È uso comune ormai rifugiarsi in montagna appena è possibile per: "Prendere una boccata d'aria fresca". Questo perché lo smog ha la caratteristica, nota a tutti, di avere un odore piuttosto sgradevole; ciò che non tutti sanno è che gli intermedi e i prodotti finali delle reazioni che avvengono al suo interno sono dannosi per la nostra salute.
Questo ha portato i paesi più civilizzati a prendere le misure opportune per migliorare la qualità dell'aria: col tempo gli effetti di questa politica iniziano a farsi sentire, ma non si può dire lo stesso dei paesi in via di sviluppo nei quali lo smog aumenta in maniera preoccupante.
Una delle caratteristiche principali della nostra atmosfera è che rappresenta un ambiente fortemente ossidante a causa della massiccia presenza di ossigeno in forma biatomica (O2). Le conseguenze sono che quasi tutti i composti gassosi (inquinanti e non) che vengono liberati nell'aria finiscono per essere ossidate da essa mentre i prodotti secondari di tali reazioni si depositano sulla superficie terrestre. Le reazioni di ossidazione sono quindi di fondamentale importanza per la qualità dell'aria.
Origini dello Smog fotochimico
Un indice assai significativo della presenza di smog è la concentrazione di ozono (O3) a bassa quota. Infatti, mentre negli strati più alti dell'atmosfera è vitale per la sua funzione di filtro alle radiazioni ultraviolette, la sua eccessiva presenza a basse altitudini è conseguenza di reazioni fotochimiche a carico degli inquinanti. Questo fenomeno è chiamato smog fotochimico, un processo che implica centinaia di reazioni che avvengono contemporaneamente. Per la prima volta fu osservato a Los Angeles negli anni '40 e in seguito a numerosi studi sulla qualità dell'aria della città sono stati fissati, in tutto il mondo, limiti alla concentrazione di ozono nell'aria. Per citare alcuni esempi ricordiamo i valori standard di USA (120 ppb), Canada (82 ppb) o OMS (Organizzazione Mondiale per la Sanità) con 100 ppb.
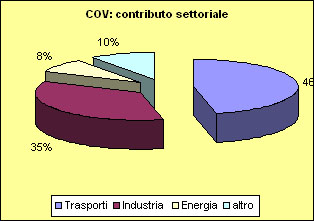
I principali responsabili del processo appena descritto sono ossido di azoto (NO) e molecole di idrocarburi incombusti emessi dagli scarichi dei veicoli con motori a combustione interna. La differenza di concentrazione di questi prodotti tra aria inquinata e non è di vari ordini di grandezza, è quindi lampante come le automobili abbiano un ruolo fondamentale nella produzione di smog. Insieme a questi occorre valutare anche i cosiddetti COV, composti organici volatili, cioè sostanze che comprendono idrocarburi e derivati ed evaporano con estrema facilità; infine la stessa luce solare ha un ruolo negativo in questa catena: aumenta la concentrazione di radicali liberi, i quali partecipano attivamente ai processi chimici di formazione dello smog.
I prodotti più rilevanti delle reazioni sono il già citato ozono, acido nitrico (HNO3), composti organici in parte ossidati ed a volte anche nitrati (NO3 ).
Per ricordare la differenza tra questi inquinanti è uso comune dividerli in due grandi gruppi:
- Inquinanti primari, di cui fanno parte ossidi d'azoto, idrocarburi e altri COV, sono quelli emessi inizialmente nell'aria dalle principali fonti di inquinamento.
- Inquinanti secondari, tra i quali ozono e HNO3, sono i prodotti della reazione fotochimica.
Esistono numerose condizioni, più o meno precise, per lo sviluppo dello smog fotochimico in un determinato territorio.
Anzitutto, il traffico veicolare deve essere intenso al punto da raggiungere quantità sufficienti di inquinanti primari; in secondo luogo occorre un clima caldo e una intensa irradiazione solare perché le reazioni cruciali per la formazione dello smog possano avvenire velocemente. Infine, la massa di aria interessata deve essere relativamente ferma, per non consentire la diluizione dei reagenti (ad esempio aree circondate da monti, i quali bloccano lo spostamento dell'aria).
Oltre alla collocazione geografica ovviamente incide pesantemente la densità della popolazione, per questo grandi città come Los Angeles, Città del Messico, Tokyo, Atene, Roma sono tra le più probabili produttrici di smog.
Soprattutto in questi luoghi ad alto rischio è importante monitorare la qualità dell'aria, ma anche fissare dei limiti e farli rispettare! Nel 1990 Città del Messico superò i limiti OMS per 310 giorni su 365: contemporaneamente si stimò che lo smog della città era sicuramente causa di migliaia di morti premature l'anno...
Per arginare questo problema le principali città interessate hanno iniziato e diminuire la circolazione veicolare durante i giorni più a rischio, ma non si può parlare di soluzione efficace.
I problemi non si fermano alle grandi metropoli: inquinanti primari e secondari infatti possono essere trasportati dalle correnti d'aria per svariati chilometri, in questo modo anche zone rurali (responsabili di emissioni limitatissime di inquinanti) si trovano con valori di inquinamento uguali o a volte maggiori delle grandi città! E i danni sono se possibile maggiori, poiché in queste aree, spesso dedicate all'agricoltura, certi tipi di coltivazioni diventano impossibili!
Come nasce lo smog: il Ciclo Fotolitico
Il principale processo del ciclo fotolitico implica una fase di produzione ed una di rimozione dell'ozono da parte degli ossidi di azoto ma da quanto verificabile sperimentalmente questi non sono sufficienti a spiegare le elevate concentrazioni di O3 osservate nelle aree urbane, bisogna quindi per forza considerare le complesse e poco studiabili reazioni che coinvolgono anche i COV.
La descrizione del complesso fenomeno di formazione dello smog fotochimico si avvale di modelli teorici che descrivono le principali reazioni coinvolte e gli stati di equilibrio conseguenti più o meno complessi la cui completezza non ne riesce a spiegare tutti gli aspetti coinvolti. Schematicamente si può quindi descrivere il tutto come segue:
gli idrocarburi vengono ossidati e la loro concentrazione aumenta nel sistema;
i radicali formatisi per ossidazione di R- ed RCO- convertono rapidamente NO in NO2, la concentrazione di NO2 sale mentre quella di NO scende;
quando la concentrazione di NO si avvicina a zero il normale processo di eliminazione dell'ozono non interviene e aumenta la concentrazione do O3 nell'atmosfera;
compaiono e aumentano le concentrazioni degli inquinanti secondari, prodotti dall'ossidazione di idrocarburi;
quando la concentrazione di NO diventa sufficientemente bassa i radicali perossiacetilici possono reagire con NO3.
In particolare a causa della reazione (c) si ha l'impossibilità della coesistenza in grandi concentrazioni di O3 e di NO. La concentrazione di O3, se presente, tende a ridursi in vicinanza di sorgenti di NO, come strade ad alta densità di traffico.
I principali inquinanti
Di seguito proponiamo una scheda per ognuno degli inquinanti menzionati precedentemente descrivendone le origini, le reazioni caratteristiche, i rischi causati dall'esposizione continua e i metodi chimici usati per la loro rilevazione.Ossidi di Carbonio (COx)
Gli ossidi di carbonio sono i tipici prodotti derivanti dalla combustione, sono incolori e inodori. La CO2 (anidride carbonica) è anche un costituente naturale dell'aria che, per la sua capacità di assorbire i raggi infrarossi, gioca un ruolo importante per il bilancio termico dell'atmosfera terrestre. Il CO (ossido di carbonio) viene prodotto in modo consistente durante la combustione di combustibili con difetto di aria e cioè quando il quantitativo di ossigeno non è sufficiente per ossidare completamente le sostanze organiche a CO2 ed H2O, ciò avviene in modo consistente e sistematico in combustioni effettuate a volume costante come quella che avviene nei motori a scoppio.
Quindi l'anidride carbonica ( biossido di carbonio) e l'ossido di carbonio ( monossido di carbonio), vengono generati sia antropicamente che naturalmente durante un processo di combustione che, se condotto in modo corretto e completo, darebbe luogo solo a CO2 e H2O.
Industrialmente il CO è contenuto negli effluenti gassosi degli impianti di produzione dei gas di sintesi per la produzione di idrogeno, metanolo e nella rigenerazione dei catalizzatori.
Reazioni caratteristiche a livello atmosferico
Gli ossidi di carbonio sono composti generalmente piuttosto stabili tanto che le uniche reazioni, non interessanti le loro interazioni con le grandi biomasse ambientali (mari, vegetazione, inerti), avvengono a livello della troposfera e sono fondamentalmente volte alla conversione di CO in CO2, grazie alla azione di radicali perossidrilici e idrossilici formatisi da reazioni fotochimiche:
Effetti sull'ambiente e sull'uomo
Elevate quantità di CO sembra portino ad una riduzione della capacità di fissare l'azoto da parte dei batteri presenti sulle radici delle piante con conseguente ridotta capacità di sviluppo della vegetazione.
L'organismo umano nella sua funzione respiratoria è largamente indipendente dalle variazioni rilevate del livello di CO2 in atmosfera e quindi generalmente per questo motivo non viene analizzata sistematicamente. In in ambienti chiusi, al contrario, la CO2 potrebbe diventare un potenziale veleno, il suo accumulo crea fenomeni di soffocamento progressivo e già a concentrazione eccedenti il 6% all'insorgere di danni acuti.
Per la vegetazione quantitativi attorno all' 1% non sono dannosi anzi portano ad incrementare l'assimilazione e quindi ad un aumento della crescita.
Per quanto riguarda gli effetti del CO sulla salute umana è nota la sua pericolosità data dalla capacità di fissarsi a livello emoglobinico circa 200 volte maggiore di quella dell'ossigeno. Questo porta ad una immediata riduzione delle capacità vitali e di conseguenza, permanendo in zone in cui il CO sia presente in quantità elevate, la morte, motivo per cui il suo essere inodore lo rende un micidiale killer.
Metodi di rilevazione
Il metodo di riferimento è il metodo automatizzato ad assorbimento IR fondato sull'assorbimento della radiazione di lunghezza d'onda intorno a 4600 nm. La variazione d'intensità è proporzionale alla concentrazione del monossido di carbonio. Il rivelatore misura differenze quantitative nella radiazione emergente dalla cella di misura rispetto a quella emergente dalla cella di riferimento contenente un gas che non assorbe radiazione nel campo IR. Le interferenze dovute a CO2 ed umidità devono essere eliminate con dispositivi adatti o strumentalmente.
Ossidi di Azoto (NOx)
Con il termine NOx vengono indicati genericamente l'insieme dei due più importanti ossidi di azoto a livello di inquinamento atmosferico ossia l'ossido di azoto, NO, e il biossido di azoto, NO2 , gas bruno di odore acre e pungente.
L'ossido di azoto, NO, è formato principalmente per reazione dell'azoto contenuto nell'aria (c.ca.70% N2 ) con l'ossigeno atmosferico in processi che avvengono ad elevata temperatura e in special modo durante le combustioni per la produzione di calore, vapore, energia elettrica, energia meccanica (autotrazione, esplosioni), incenerimento, ecc... .
Una volta formatosi, l'ossido di azoto, interagendo con l'ossigeno durante il processo di raffreddamento dei fumi, sempre in eccesso in un processo di combustione, si trasforma parzialmente in biossido di azoto con formazione di un miscuglio dei due ossidi chiamato NOx.
Entrambe le suddette reazioni sono strettamente correlate con la temperatura, con il residuo di ossigeno presente ed, in particolare per il biossido di azoto, con [NO]2( quadrato della concentrazione del monossido). In generale si può ritenere che la produzione di NO2 , quale inquinante primario, sia pari al 10 % dell'ossido di azoto complessivamente generato.
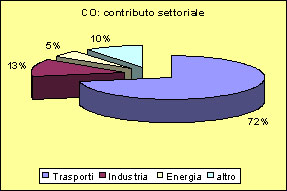
Il maggiore responsabile dell'inquinamento antropico da ossidi di azoto è il traffico autoveicolare che rappresenta quasi il 50% della produzione globale ed in particolare per l'utilizzo dei motori diesel, insieme alle attività industriali della zona considerata.
Industrialmente infatti questi inquinanti possono essere emessi dagli impianti di produzione dell'acido nitrico e da quelli che lavorano composti azotati o che utilizzano direttamente l'acido nitrico come composto base come per la produzione di fertilizzanti, come acido adipico e nylon 6.6, per fare qualche esempio.
Le Reazioni caratteristiche a livello atmosferico
La notevole reattività fotochimica è sicuramente la caratteristica peculiare degli ossidi di azoto. Le reazioni fotochimiche, come accennato precedentemente, avvengono in seguito all'assorbimento di energia proveniente dalla radiazione solare da parte di molecole, atomi e ioni. Questo tipo di reattività li rende precursori di una innumerevole serie di reazioni radicaliche che avvengono nella troposfera le cui fondamentali sono riassunte nel "Ciclo Fotolitico".
Durante questo ciclo, se non intervenissero altri fattori, si manterrebbero costanti i rapporti tra NO2 e NO presenti in atmosfera. In realtà la presenza di altre molecole accettrici di radicali, quali ad esempio particolari idrocarburi, favoriscono l'accumulo di NO2 e di ozono, O3. Ulteriori reazioni non ancora completamente studiate sono quelle che portano nel giro di tre, quattro giorni alla scomparsa completa sia di NO che di NO2, si pensa per la loro trasformazione in presenza di umidità atmosferica in acido nitrico e di conseguenza in nitrati che ricadono poi al suolo con le piogge o sotto forma di particolati.
Effetti sull'ambiente e sull'uomo
I maggiori effetti diretti sull'ambiente degli ossidi di azoto sono dovuti alla loro ricaduta sotto forma di acido nitrico che creano zone di aggressione puntiformi ad elevata concentrazione, sia dagli ossidi in quanto tali. Esperimenti condotti hanno portato a verificare che 1 ppm di NO2 per 24 ore di esposizione crea già le prime necrosi a livello del fogliame, mentre 10 ppm di NO per 24 ore debilitano già in modo sensibile la fotosintesi clorofilliana.
Sull'uomo è stato riscontrato che l'NO2 pare essere 4 volte più pericoloso dell' NO ma data la facilità del loro interscambio entrambi sono potenzialmente pericolosi. Particolarmente significative sono comunque le esposizioni prolungate anche a bassi tassi di ossidi di azoto tanto che si sta studiando la possibilità che ben più importante debba essere l'apporto di ossidi di azoto respirati durante il soggiorno nelle abitazioni (inquinamento indoor) dovuto all'utilizzo dei fornelli a gas o alle caldaie di riscaldamento acqua e/o ambiente. Oltre alla loro pericolosità intrinseca, essendo questi particolarmente reattivi specialmente con sostanze di origine idrocarburica, si arriva alla formazione di composti la cui tossicità risulta fortemente amplificata.
Metodi di rilevazione
Il metodo (automatizzato) è basato sulla chemioluminescenza in seguito alla reazione tra ossido d'azoto ed ozono con produzione di biossido d'azoto eccitato che emette una radiazione elettromagnetica nel vicino infrarosso (intorno a 1200 nm). In presenza d'eccesso d'ozono l'intensità della radiazione è proporzionale alla concentrazione dell'ossido d'azoto. La radiazione emessa viene filtrata su filtro ottico selettivo e convertita da un tubo fotomoltiplicativo in segnale elettrico. La misura del biossido d'azoto viene fatta per differenza fra la misura degli ossidi di azoto totali, cioè l'ossido d'azoto contenuto nell'aria più quello proveniente dalla riduzione del biossido d'azoto, e quella del solo ossido. Per la misura dell'ossido d'azoto il campione d'aria viene inviato direttamente nella camera di reazione dove viene miscelato con ozono. Per la misura degli ossidi totali (Nox) l'aria viene fatta passare attraverso un convertitore (riduttore) che trasforma il biossido in ossido d'azoto.
Ozono (O3)
L'ozono è un gas di colore azzurro pallido, di peso molecolare circa doppio rispetto a quello dell'aria, che assorbe fortemente la radiazione solare UV (ultravioletta) nella regione spettrale da 200 a 350 nm e debolmente attorno a 600 nm risultando quindi un formidabile schermo di protezione per le temibili radiazioni ultraviolette pericolose per le forme di vita del nostro pianeta.
Nella troposfera non vi sono emissioni significative di ozono prodotte dall'uomo e l'ozono presente è di origine secondaria, ovvero prodotto naturalmente da reazioni fotochimiche che coinvolgono direttamente l'ossigeno atmosferico, reazioni attualmente enormemente amplificate dagli inquinanti immessi direttamente in atmosfera dall'uomo. Nelle aree non inquinate del pianeta le concentrazioni di fondo osservate variano da circa 40 a 160 mg/m3 , dovuto essenzialmente al trasporto di ozono dall'alta troposfera, dalla stratosfera (20-40 Km.) e da produzione locale provocata da irraggiamento solare (scarsamente significativa al livello del mare ma più significativa in quota es. in montagna); quantitativi di ozono sensibilmente inferiori vengono prodotti dalle scariche atmosferiche durante i temporali.
Nelle aree popolate del pianeta interessate dalla presenza di inquinanti primari di origine umana il principale meccanismo di produzione dell'ozono è costituito dal processo chimico-fisico che da origine al già menzionato smog fotochimico, del quale il gas può essere considerato sia il precursore che il principale tracciante.

Reazioni in atmosfera
L'ozono reagisce con i COV e NOx con reazioni alquanto complesse dando origine a radicali ed a prodotti finali anche altamente tossici quali i perossialcilnitrati (PAN) in un processo noto in letteratura come ciclo fotolitico i cui prodotti finali sono identificati genericamente con il nome di inquinanti fotochimici.
La grande importanza attribuita all'inquinamento fotochimico dipende dal fatto che il tempo di permanenza dell'ozono nell'atmosfera (qualche giornata) è lungo abbastanza da consentire la sua propagazione a grande distanza, una volta che si sia formato e ciò accade normalmente quando un anticiclone (alta pressione) si stabilizza in zone caratterizzate da intensa emissione di COV e NOx (aree urbane e altamente industriali).
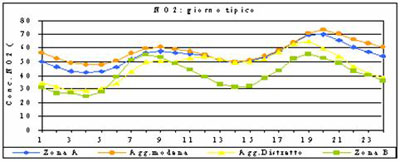
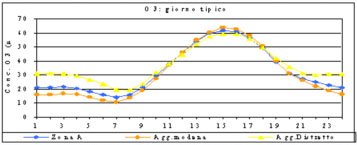
Nel ciclo giornaliero si verifica sperimentalmente che nelle ore che precedono l'alba, quando l'attività umana è al minimo, la concentrazione degli inquinanti primari è stazionaria e la concentrazione degli inquinanti secondari è ad un livello minimo. All'aumentare della attività umana inizia l'accumulare di NOx (in particolare NO) ed idrocarburi e quando l'intensità della radiazione UV diventa tale da generare quantità considerevoli di O3, l'ossido di azoto viene da questo convertito in biossido: da questo punto inizia l'aumento dell'ozono che raggiungerà il massimo a metà giornata. Mentre aumenta O3 diminuisce NO2 , calano gli idrocarburi e si accumulano aldeidi, chetoni e PAN, solo verso sera la luce non è più sufficiente per generare nuovo O3 per convertire tutto l'NO prodotto in NO2 che consumerà l'O3 accumulatosi durante la giornata facendone diminuire i livelli.
Volendo schematizzare le equazioni di reazioni più tipiche ne possiamo elencare quattro, due di formazione e due di decomposizione:
Formazione
O2 + hv1 ——» O + O
L'ossigeno atmosferico, colpito da radiazioni U.V. provenienti dal sole, assorbe l'energia sufficiente a rompere il proprio legame e sfrutta quella in eccesso come energia cinetica.
O + O2 + M ——» O3 + M
M rappresenta un qualsiasi atomo o molecola che intervenga nella reazione assorbendo l'energia cinetica dell'atomo O e consentendo la formazione del debole legame con l'ossigeno atmosferico.
Decomposizione
O3 + hv2 ——» O2 + O
I deboli legami che formano l'ozono si rompono assorbendo radiazioni di λ della zona degli infrarossi, nocivi per l'uomo. Questa è essenzialmente la funzione dell'ozono in alta atmosfera, filtrare le radiazioni aggressive provenienti dal Sole.
C'è inoltre un'ulteriore reazione di decomposizione, meno importante della precedente.
O3 + O ——»2 O2
Effetti sull'ambiente e sull'uomo
Sulle piante gli effetti dell'ozono sono segnalati da macchie o piccoli punti di necrosi cellulare sulla superficie delle foglie o da bruciature a livello dei germogli. Pare altresì che più la pianta sia ricca di zuccheri e più sia resistente all'ozono, fattore che influisce notevolmente nella determinazione del valore soglia di tossicità.
La pericolosità nei confronti dell'uomo deriva dall'alto potere ossidante della molecola di ozono e della sua capacità di giungere facilmente a livello alveolare; i primi sintomi sono irritazione degli occhi e disturbi respiratori.
Grazie alla sua reattività nei confronti delle matrici organiche appare chiaro che qualunque zona dell'apparato respiratorio è un bersaglio per questo inquinante, se una esposizione acuta crea problemi in generale risolvibili una volta cessata l'esposizione per un periodo di almeno 48 ore, una esposizione prolungata a quantitativi anche non elevati provoca fenomeni di sensibilizzazione ed irritazione persistenti.
Metodi di rilevazione
Metodo automatizzato ad assorbimento UV: il campione d'aria è inviato continuamente in una cella ottica dove viene irradiato con luce UV a 253.7 nm. L'assorbimento di questa radiazione è proporzionale alla concentrazione d'ozono. Per evitare interferenze da altri gas che possono assorbire alla stessa lunghezza d'onda e da instabilità della sorgente di luce ultravioletta, un convertitore catalitico d'ozono è utilizzato per rimuovere selettivamente l'ozono dal flusso d'aria che andrà successivamente a riempire la cella di riferimento (o la stessa cella d'assorbimento in cui verrà mandata alternativamente aria non trattata e trattata).
Composti Organici Volatili (COV)
Con la dicitura composti organici volatili, COV, si intendono tutta quella serie di composti organici, prodotti dalle attività umane o naturali, che si trovano allo stato di gas alle condizioni di temperatura e pressione esistenti a livello troposferico.
Possono essere semplici idrocarburi saturi o insaturi a molecola lineare e non, composte esclusivamente da carbonio e idrogeno, o molecole più complesse in cui , tra i più diffusi, sono presenti atomi di azoto, ossigeno e cloro.
A livello naturale si ha la presenza di 1.0-2.0 ppm di metano, la più semplice molecola organica esistente, e valori inferiori a 0.1 ppm per la totalità di tutti gli altri idrocarburi più complessi.
Questi valori sono giustificabili dall'elevato numero di processi di decomposizione biologica della materia organica dalle biomasse, quantità più modeste sono invece attribuibili ad attività geotermiche, dai giacimenti fossili, di gas naturale, e di petrolio e nei processi di combustione.
Per quanto riguarda l'introduzione di composti organici da parte dell'uomo si può affermare che la fonte maggiore è sicuramente quella dovuta al traffico autoveicolare. Infatti, mentre nei fumi di combustioni delle centrali termiche (combustione a pressione costante) il contributo all'inquinamento atmosferico in idrocarburi incombusti, o parzialmente combusti sotto forma di aldeidi o acidi organici è modesto, quello dovuto alla combustione per la motorizzazione risulta assai elevato (combustione a volume costante).
Nei processi industriali le maggiori fonti sono derivanti dai processi di verniciatura, produzione di monomeri per l'industria delle materie plastiche e alle industrie collegate alla produzione e utilizzo dell'etilene, a livello civile non sono altres� trascurabili i contributi derivanti dai processi di lavaggio tessuti e grassaggio di particolari da sottoporre al processo di verniciatura.
Reazioni in atmosfera
Essendo molto variegato il numero di possibili molecole organiche immesse in atmosfera è praticamente impossibile la descrizione e la conoscenza di tutti i processi in cui sono coinvolte, certamente il gruppo di reazioni in cui sono maggiormente implicate sono i processi fotochimici.
Ricordiamo inoltre come la produzione di un elevato numero di radicali liberi risulta determinante sia a livello del ciclo degli ossidi di azoto che per quello dell'ozono e come anzi tutte queste reazioni siano direttamente correlate.
Effetti sull'ambiente e sull'uomo
Per la flora gli idrocarburi più nocivi sono soprattutto quelli difficilmente metabolizzabili che danno di conseguenza fenomeni di accumulo con i problemi connessi.
Sull'uomo gli effetti sono dovuti fondamentalmente o a macromolecole delle quali si conoscono i possibili effetti sulla salute umana, ad esempio pireni e policiclici aromatici in genere, IPA, o a molecole attivate per reazione fotochimica e che quindi, essendo generalmente piuttosto reattive svolgono un'azione di sicuro interesse tossicologico, oppure molecole tal quali di cui si conoscono gli effetti nocivi quale può essere il benzene.
Interessante è notare che la maggior azione a livello tossicologico viene espletata qualora questi composti siano supportati su pulviscolo o particolato che funge da substrato di trasporto per una sua introduzione permanente a livello polmonare.
Metodi di rilevazione
Il metodo (non utilizzabile per il metano) è il metodo automatizzato che fa uso di un rivelatore a ionizzazione di fiamma. Ogni ciclo di misura consta di due fasi: nella prima un volume noto di aria viene inviato direttamente al rivelatore in modo da ottenere il segnale corrispondente agli idrocarburi totali; nella fase successiva arriva al rivelatore l'effluente dalla colonna gascromatografica nella quale viene iniettato periodicamente un eguale volume d'aria e separato il metano dagli altri idrocarburi (alcuni tipi di analizzatori sono provvisti di doppio rivelatore per la misura contemporanea di metano ed idrocarburi). Costruite le curve di taratura per metano e idrocarburi (si utilizzano miscele campioni contenenti concentrazioni note di metano e butano) si risale alle concentrazioni di idrocarburi non metanici per differenza.
Particolati
I particolati sono le minuscole particelle solide o liquide sospese nell'aria che di solito, prese singolarmente, sono invisibili ad occhio nudo, mentre nel loro insieme formano una foschia che riduce la visibilità. Un aerosol è un insieme di particolati (solidi e liquidi) dispersi nell'aria, ma spesso il termine è utilizzato anche impropriamente (ad esempio parlando di spray spruzzato da una bomboletta), il vero aerosol è formato da particelle molto piccole, con diametri inferiori a 0,0001 m, cioè 100 μm.
Le particelle presenti sono indicate con molti nomi comuni: polvere e fuliggine sono riferiti a particelle solide, mentre caligine e nebbia corrispondono a sospensioni acquose (nel secondo caso sono goccioline di acqua molto concentrate).
Vengono definite absorbite sostanze che si disciolgono all'interno di una particella, mentre se tra le due si instaura solo un legame superficiale si parla di adsorbimento.
Un esempio importante e assai diffuso del secondo caso è quello dell'adsorbimento di grosse molecole organiche da parte di particelle di carbonio, la famosa fuliggine, ed in effetti è proprio il carbonio a formare la maggior parte della massa di sospensione solida nell'aria.
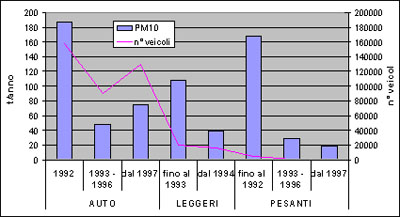
Una delle sue fonti più importanti è rappresentata dalle emissioni dei motori diesel, per questo dal 1994 è iniziata una rigida campagna di controllo delle emissioni e di regolamentazioni, come l'obbligo per camion e autobus di installare dispositivi per il trattamento di gas combusti.
Ma qual è il destino di queste sospensioni una volta emesse? Intuitivamente viene spontaneo pensare che tutte le particelle dovrebbero sedimentare velocemente al suolo per gravità, ma ciò non accade per quelle più piccole. Si è scoperto infatti che la velocità (spazio percorso nel tempo) a cui le particelle sedimentano aumenta con il quadrato del loro diametro.
Ciò significa che un particolato il cui diametro sia la metà di un altro sedimenterà ben quattro volte più lentamente, quindi per le particelle più piccole di sospensione è possibile ipotizzare una permanenza pressochè indefinita, a meno che non si uniscano a qualche altra particella di dimensioni maggiori.
Le particelle con diametro inferiore a 2,5 μm sono dette polveri fini e solitamente rimangono in sospensione per giorni o settimane; quelle di diametro maggiore sono dette polveri grossolane e sedimentano piuttosto rapidamente.
Oltre che per sedimentazione, le particelle vengono allontanate dall'aria anche per absorbimento nelle goccioline di pioggia.
Il particolato grossolano in particolare non è quasi mai originato da reazioni chimiche, ma si crea soprattutto durante processi più o meno naturali, come le eruzioni vulcaniche o la frantumazione di pietre nelle cave. Confrontate con le parti più fini queste ultime sono meno pericolose per svariati motivi:
Data la loro dimensione, sedimentano molto più velocemente diminuendo il potenziale tempo di esposizione all'uomo.
Se inalate, particelle di queste dimensioni vengono efficacemente filtrate dalle mucose nasali e nella gola, non permettendo il contatto con i polmoni. Altrettanto non accade per quelle fini che, una volta inalate, arrivano quasi sempre ai polmoni dove vengono adsorbite dalla superficie cellulare (per questo sono dette respirabili).
Le tecnologie finora utilizzate per abbattere l'aerosol (precipitatori elettrostatici, camere da filtri) sono efficaci solo per le particelle di maggiori dimensioni.
Il parametro atto a misurare la concentrazione dei particolati nell'aria era definito in passato PTS (particolato totale in sospensione), l'unità di misura adottata era μg/m³ cioè massa di particelle per volume di aria. Non è possibile parlare di concentrazioni molari poiché, data la eterogeneità delle molecole, non è possibile fissare una massa molare.
Un valore standard comunemente accettato per questo PTS è 75 μg/m³, ma non è molto indicativo: siccome solo le frazioni più piccole sono respirabili, sarebbe più appropriato un indice che rappresenti la concentrazione delle sole particelle respirabili per l'uomo.
Per questo è stato accettato un nuovo tipo di misurazione detto PM10, il quale misura la concentrazione delle sole polveri con diametro minore di 10 μm, come indice di rilevanza ambientale del particolato.
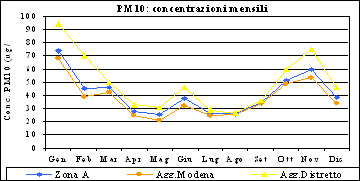
Un'altra tecnica di uso comune per misurare l'entità di questo tipo d'inquinamento è la nebbiosità. Le particelle con diametro simile alla lunghezza d'onda della luce visibile, infatti, possono interferire con il passaggio della luce nell'aria, diminuendone la chiarezza, la visibilità a lunga distanza e le quantità di luce che raggiunge il suolo. Accade quindi che elevate concentrazioni di particelle del diametro di 0,1-1 μm producano una foschia. Per esempio quella che si registra nell'artico durante la stagione invernale è originata dalle consistenti combustioni di carbone in Russia ed Europa e al conseguente aerosol di acido solforico.
Altre particelle fini sono anche responsabili in gran parte delle foschie che si registrano sulle principali località affette da smog fotochimico.
Reazioni in atmosfera
Qualora il particolato sia costituito da sostanze chimicamente attive, queste danno luogo a tutte quelle reazioni superficiali caratteristiche per i composti che lo costituiscono.
Di notevole e maggiore interesse è pero la capacità anche di particolati inerti di adsorbire sostanze che si rendono così disponibili a reazioni con elevata reattività in quanto allo stato micronizzato e attivato.
Non a caso il particolato creato dagli autoveicoli è ben più pericoloso di quello dovuto alle industrie poiché sul primo, generalmente particelle carboniose, possono essere adsorbiti tutta una serie di inquinanti, soprattutto organici, che vengono quindi dispersi su un supporto particolarmente efficace sia come catalizzatore intrinseco che come veicolo di trasporto ai polmoni, mentre in generale i processi industriali danno granulometrie più grosse che quindi permangono per un minor tempo in atmosfera.
In generale le polveri derivano comunque da attività umane come processi industriali, impianti di riscaldamento e naturalmente traffico veicolare. A differenza dei precedenti inquinanti però, oltre che dai gas di scarico possono avere origine anche con l'erosione del manto stradale e l'usura di pneumatici e di freni.
Effetti sull'ambiente e sull'uomo
Gli effetti ambientali del particolato sono direttamente connessi con la pericolosità intrinseca delle sostanze che lo formano o che sono adsorbite su di esso. Particolari effetti vengono riscontrati sulla vegetazione che risente in maniera sensibile sia delle particelle di polvere in quanto tali che di molte delle sostanze che su di esse si trovano adsorbite, metalli, sostanze organiche e altre.
Sembra comunque che anche il pulviscolo inerte con diametro inferiore a 20m , qualora la concentrazione superi la media annuale di 0.1 mg/m³ determini una maggiore incidenza di infiammazioni croniche delle vie aeree, riniti faringiti, laringiti, bronchiti.
Gli effetti sull'uomo quindi sono evidenti tanto più le particelle sono piccole ed attive sia chimicamente che per la loro struttura (quarzo) o forma (amianto), in quanto superate le barriere naturalmente create dal nostro organismo si annidano a livello delle mucose polmonari per parecchio tempo dando cosi la possibilità ad eventuali reazione nocive di instaurarsi nelle condizioni più favorevoli. È stato provato che le particelle più minute hanno la capacità di superare completamente la mucosa respiratoria ed entrare direttamente nel circolo sanguigno.
Metodi di rilevazione
Un campionatore d'aria aspira l'aria atmosferica a flusso costante attraverso un sistema d'ingresso dell'aria di geometria particolare in cui il materiale particolato sospeso viene separato inerzialmente in una o più frazioni dimensionali entro l'intervallo PM10. Ciascuna frazione dimensionale viene quindi raccolta su filtri separati durante il periodo di campionamento stabilito (24 ore più o meno 1). La frazione PM10 viene determinata gravimetricamente per differenza tra il peso del filtro prima del campionamento e dopo (i filtri devono essere condizionati prima e dopo il prelievo per l'umidità).
Benzene
Il benzene è una sostanza chimica liquida ed incolore dal caratteristico odore aromatico pungente. A temperatura ambiente volatilizza assai facilmente, cioè passa dalla fase liquida a quella gassosa. A causa dell'elevato contenuto di carbonio, il composto puro brucia producendo notevoli quantità di fumo, tuttavia una miscela di benzene e benzina costituisce un buon carburante. In Europa miscele di benzene, toluene, o altri composti simili, sono state per lungo tempo aggiunte alle benzine.
Ha un odore caratteristico e molto forte e, se inalato in quantità elevate, è tossico e cancerogeno; è inoltre facilmente infiammabile e produce vapori esplosivi.
Il benzene presente nell'aria deriva da processi di combustione incompleta sia di natura antropica (emissioni industriali, veicoli a motore), che naturale (incendi). Tra queste, la maggiore fonte emissiva è costituita dai gas di scarico dei veicoli a motore, alimentati con benzina (principalmente auto e ciclomotori). Il benzene rilasciato dai veicoli deriva dalla frazione di carburante incombusto, da reazioni di trasformazione di altri idrocarburi e, in parte, anche dall'evaporazione che si verifica durante la preparazione, distribuzione e stoccaggio delle benzine, ivi comprese le fasi di marcia e sosta prolungata dei veicoli.
I livelli ambientali di benzene sono abbastanza bassi da non far temere la comparsa delle patologie denunciate in passato nei luoghi di lavoro, ma le informazioni a disposizione non sono ancora sufficienti per concludere che l'effetto complessivo sia trascurabile. L'esposizione prolungata a bassi livelli di benzene è infatti correlata ad un aumento nella frequenza di insorgenza del cancro negli uomini.
La guida di autoveicoli comporta un'esposizione proporzionale al tempo di guida, che risulta di circa 3-4 volte superiore a quella ambientale generale.
L'importanza del traffico autoveicolare come fonte di inquinamento è testimoniata dal fatto che in popolazioni rurali la concentrazione di benzene nel sangue risulta significativamente più bassa rispetto a quella di chi vive in città.
Reazioni ed Usi

Il benzene è uno dei composti organici più utilizzati divenne disponibile in grandi quantità a partire dal 1842, quando fu messo a punto un metodo per estrarre questa sostanza dal catrame di carbone (una tonnellata di carbone fornisce circa 8 litri di benzene). Attualmente il liquido viene prodotto dalla lavorazione del petrolio, sia per estrazione diretta da alcuni oli grezzi sia per trattamento chimico (hydroforming).
Su scala industriale viene prodotto attraverso processi di raffinazione del petrolio e trova impiego principalmente nella chimica come materia prima per numerosi composti secondari, che a loro volta vengono utilizzati per produrre plastiche, resine, detergenti, pesticidi. È un costituente della benzina, dove viene utilizzato come antidetonante in sostituzione del piombo. In Italia la legge n. 413/97 ha stabilito che il contenuto di benzene nelle benzine non deve superare l'1% in volume.
Effetti sulla salute
Il benzene è facilmente assorbito per inalazione, contatto cutaneo, ingestione, sia per esposizione acuta che cronica. Gli effetti tossici, tuttavia, hanno caratteristiche diverse e colpiscono organi sostanzialmente differenti in base alla durata dell'esposizione.
Si possono distinguere effetti tossici acuti, associati a brevi esposizioni a livelli elevati di benzene, poco frequenti nell'ambiente di vita, ed effetti tossici cronici, associati a periodi di esposizione di maggiore durata e a basse dosi di inquinante.
L'intossicazione acuta accidentale da benzene fa seguito generalmente ad esposizione per via inalatoria e/o cutanea. Per esposizione acuta, gli organi bersaglio sono il sistema nervoso centrale (con cefalea, nausea, vertigine, ecc.) ed il miocardio.
L'effetto più noto dell'esposizione cronica riguarda la potenziale cancerogenicità del benzene sul sistema emopoietico (cioè sul sangue).
L'Agenzia Internazionale per la Ricerca sul Cancro (IARC) classifica il benzene come sostanza cancerogena di classe I, in grado di produrre varie forme di leucemia. La classe I corrisponde ad una evidenza di cancerogenicità per l'uomo di livello "sufficiente".
Metodi di rilevazione
Una colonna gascromatografica tipo DB1 esegue la separazione cromatografica ed un rivelatore a spettrometria di massa operante in SIM (rivelazione selettiva di ioni) identifica il picco del benzene per confronto dei tempi di ritenzione assoluto e relativo rispetto al benzene perdeuterato. La determinazione quantitativa è compiuta per confronto con il metodo dello standard interno.
Metalli
Con questa denominazione si raggruppano una serie di elementi metallici che si ritrovano nel particolato atmosferico a seguito del loro adsorbimento come da parte del piombo generato dal traffico autoveicolare o di specifici metalli immessi direttamente dalle industrie che li utilizzano nei più svariati processi produttivi, che come parte integrante o inquinante del materiale stesso areodisperso.
Reazioni in atmosfera
Generalmente considerati come facenti parte del particolato non sono responsabili di particolari reazioni a livello atmosferico a causa della loro necessaria attivazione se presenti allo stato metallico o per la necessaria presenza di ulteriori molecole per le quali si comportano in generale come catalizzatori per la produzione di composti nocivi.
Effetti sull'ambiente e sull'uomo
I loro effetti sull'ambiente sono sostanzialmente diversi a seconda del tipo di metallo considerato e la così grande casistica non ci permette di darne una visione di assieme. Per quanto riguarda la salute dell'uomo ci limitiamo invece a considerare i metalli più indicativi con i loro effetti.
| Metallo | Fonte Principale | Effetto |
|---|---|---|
| Nichel | Nafta, olii, acciao, leghe | Cancro polmonare |
| Boro | Carbone, vetrerie, ceramiche | Non tossico se non sotto forma di borani |
| Arsenico | Carbone, petrolio | Può causare cancro |
| Mercurio | Carbone, pile | Danni al sistema nervoso, a volte morte |
| Cadmio | Carbone, lavorazione zinco | Sospetta causa di malattie cardiovascolari, ipertensione |
| Piombo | Benzina Super | Danni al cervello, convulsioni |
Metodi di rilevazione (Piombo)
Il piombo contenuto nel materiale particellare sospeso viene raccolto filtrando un volume noto di aria per almeno 24 ore attraverso un filtro a membrana a micropori (pompa che consenta di regolare e mantenere la portata di aspirazione a 20 litri/minuto più o meno 5%). Dopo mineralizzazione del filtro con acido nitrico si determina il piombo nella soluzione per spettrofotometria di assorbimento atomico (i filtri devono essere condizionati prima e dopo il prelievo per l'umidità).
Cloro Fluoro Carburi
Le prime avvisaglie dell'assottigliamento della fascia di Ozono risalgono al 1974. Due scienziati Nord americani affermarono che i gas conosciuti come Cloro Fluoro Carburi avrebbero alla lunga rappresentato un serio pericolo per la Terra se non si fossero prese delle contromisure.
Fino ad allora i CFC erano stati considerati prodotti chimici perfetti. Erano inodori, non erano tossici né infiammabili e chimicamente erano inerti.
Per questa loro "affidabilità" vennero a lungo impiegati nei frigoriferi e nei condizionatori d'aria, nei solventi chimici per la pulitura a secco, nelle plastiche espanse (tipo i contenitori per gli hamburger) e in moltissimi altri settori industriali, non ultimo quello cosmetico dove sono stati a lungo impiegati come propellenti nelle bombolette spray.
I CFC sono gas talmente "stabili" da poter rimanere in sospensione nell'atmosfera anche più di cento anni prima di raggiungere la stratosfera dove iniziano a distruggere le molecole di Ozono che proteggono la terra dalle radiazioni solari.
Fino al 1985 la stessa comunità scientifica è stata divisa sulla portata reale del fenomeno, ma la scoperta di un vero e proprio "buco" nella fascia di Ozono sovrastante l'Antartide spinse la comunità mondiale a prendere misure effettive di contenimento del fenomeno.
Nel 1987 venne firmato a Montreal un protocollo in cui 23 paesi, tra cui l'Italia, si impegnavano a ridurre del 30% entro il 1999 il consumo di CFC.
Dopo il protocollo di Montreal è iniziato un ampio dibattito a riguardo delle alternative ai CFC. Numerosi sono i punti che devono essere considerati attentamente, come ad esempio l'impoverimento dell'Ozono, il riscaldamento globale, l'infiammabilità e la tossicità. Poiché non esistono fluidi che soddisfino contemporaneamente tutti e quattro i requisiti, occorre essere consapevoli delle scelte che si fanno. La tendenza é quella di seguire due linee di sviluppo: una rivolta verso l'utilizzo degli idrocarburi fluorurati mentre l'altra privilegia i fluidi naturali come l'ammoniaca, il propano, il butano, la CO e l'acqua.
Da parecchio tempo in molte nazioni i fluidi CFC completamente alogenati contenenti cloro costituiscono il principale problema. Ma in alcune nazioni anche l'anticipata fase di dismissione degli HCFC costituisce un problema. Tra i nuovi refrigeranti solo l'R134a risulta essere accettabile in tutto il mondo come fluido di lavoro. L'importanza di nuovi fluidi come l'ammoniaca sta aumentando specialmente per il fatto che altre alternative sono, ad esempio, infiammabili o comportano alte pressioni di lavoro. Per evitare tali inconvenienti vengono utilizzate miscele che però presentano un più alto potenziale di riscaldamento globale. Il principale obbiettivo è, quindi, quello di minimizzare i diversi rischi.
Caratteristiche dei refrigeranti
L'impatto dei refrigeranti sull'ambiente può essere sintetizzato nei seguenti punti:
- Tossicità nei riguardi dell'uomo e degli animali
- Influenze biologiche e genetiche
- Odori
- Infiammabilit� ed esplosività
- Impatto diretto sul riscaldamento globale
- Consumi energetici durante la produzione e l'utilizzazione e impatto sulla produzione di CO
- Possibile influenza sullo strato d'Ozono
- Tensione di vapore
- Entalpia d'evaporazione
- Capacità frigorifera specifica
- Conducibilità del calore
- Viscosità
- Tensione superficiale
- Solubilità con gli oli
- Corrosività
- Stabilità
Dalla loro introduzione sul mercato pi� di 60 anni fa, i CFC sono sempre stati considerati dei fluidi stabili e non tossici. Oggigiorno la loro scarsa reattività con altre molecole può risultare avere effetti negativi sull'effetto serra. L'impatto sull'ambiente dei diversi tipi di refrigeranti puà essere sintetizzato attraverso la creazione di quattro diversi gruppi di fluidi derivati dagli idrocarburi:
I CFC (cloro-fluoro-carburi), completamente alogenati e privi di idrogeno nella molecola (ad esempio R11, R12, R12B1)
Gli HCFC (idro-cloro-fluoro-carburi), parzialmente alogenati e contenenti idrogeno nella loro molecola (ad esempio R22)
Gli FC (fluoro-carburi) aventi una molecola formata solamente da atomi di cloro e di fluoro (ad esempio R14,R116,RC318)
Gli HFC (idro-fluoro-carburi) parzialmente alogenati, privi di cloro, e contenenti idrogeno nella molecola (ad esempio R32, R125, R134a, R227, R245)
Oggigiorno l'impatto sull'atmosfera, ossia il potenziale impoverimento sull'Ozono e l'impatto sul riscaldamento globale, rappresenta un problema molto rilevante. L'utilizzo di questi refrigeranti richiede, comunque, di considerare tutte le possibili conseguenze. La tabella 1 mostra i valori relativi, preso come riferimento l'R11, del potenziale di impoverimento dell'Ozono (ODP) e del potenziale di riscaldamento globale (GWP) per R11, R12 e i loro più probabili sostituti.
Tabella 1: proprietà dei refrigeranti
| ODP (R11=1) |
GWP (CO =1) |
Tossicità | Infiammabilità | |
| R11 | 1 | 4000 | No | No |
| R12 | 1 | 8500 | No | No |
| R22 | 0,055 | 1700 | No | No |
| R32 | 0 | 580 | (no) | Si |
| R125 | 0 | 3200 | (no) | No |
| R142b | 0,0065 | 2000 | (no) | No |
| R143a | 0 | 4400 | No | (si) |
| R134a | 0 | 1300 | No | No |
| R152a | 0 | 140 | No | Si |
| R227 | 0 | 2900 | No | No |
| R717 (ammoniaca) |
0 | 0 | Si | (no) |
| R290 (propano) |
0 | 3 | No | Si |
| R600 (butano) |
0 | 3 | No | Si |
| R718 (acqua) |
0 | 0 | No | No |
| R744 (CO ) |
0 | 1 | No | No |
| Elio | 0 | 0 | No | No |
Il cloro è causa di problemi per lo strato d'Ozono e, data la stabilità delle sue molecole, provoca un aumento del surriscaldamento globale della Terra. La presenza di idrogeno nella molecola, conferisce maggiore instabilità ai composti e può portare alla formazione di fluidi infiammabili. Se si desidera evitare l'impoverimento dello strato d'Ozono atmosferico è necessario utilizzare o fluidi potenzialmente infiammabili (contenenti fluoro e idrogeno) o fluidi che comportano un potenziale di riscaldamento globale della Terra. L'utilizzo dei fluidi refrigeranti comporta inevitabilmente lo scontrarsi con uno di questi due problemi. La decisione, in questi termini, deve essere presa a livello politico, poiché da un lato siamo di fronte ad una questione di carattere ecologico, ma dall'altra ci scontriamo con un problema inerente la sicurezza del genere umano. Il potenziale cui si fa riferimento nelle sigle ODP e GWP si riferisce agli effetti possibili, non a quelli già verificatesi. In altre parole, l'ODP e il GWP acquistano rilevanza pratica solo quando e se i refrigeranti vengono rilasciati in atmosfera. Di conseguenza assumono molta importanza le misure preventive contro fughe e i rilasci di refrigeranti, così come le procedure di riciclaggio degli stessi. La perfetta ermeticità degli impianti e le operazioni di recupero dei refrigeranti possono significativamente ridurre non solo l'impatto sul riscaldamento globale ma anche sull'impoverimento dello strato di Ozono.
Nuovi sostituti per i CFC non appartenenti alla famiglia degli idrocarburi alogenati
Anche se l'R134a viene utilizzato su larga scala in tutto il mondo, permane vivo il dibattito sui sostituti dei CFC e dell'R22 a medio e lungo termine. Le alternative disponibili quando l'R22 verrà bandito sono:
| Per R11 | R123R216R245ca R356 |
R245fa |
| Per R12 | R152aR227ca R245cb |
R227ea R134a |
| Per R502 | R125 R143a |
R507 (R125/R143a50/50) |
| Per R22 | R143a R410A (R32/R12550/50) R407C (R32/R125/R134a23/25/52) |
R32 |
Poiché l'R32 è infiammabile, sono state sviluppate molte miscele con fluidi non infiammabili. Tali miscele binarie o ternarie, non infiammabili, presentano un potenziale di riscaldamento globale superiore a quello dell'R22.
Utilizzo degli idrocarburi
In alcune nazioni, soprattutto europee, viene data molta rilevanza al GWP di un fluido, tanto che si preferiscono refrigeranti con basso o nullo GWP anche se essi sono infiammabili, come ad esempio propano, butano, isobutano o pentano. Essi, oltre ad avere un GWP nullo presentano il grosso vantaggio di avere anche un OPD nullo.
In Germania vengono prodotti giornalmente alcune migliaia di frigoriferi domestici funzionanti con idrocarburi. Essi utilizzano come refrigerante propano o miscele di propano e isobutano. Anche l'isobutano puro viene utilizzato con buon successo. La quantità di isobutano in un frigorifero da 130 litri si aggira attorno ai 20 grammi, di cui 12 risultano dissolti nell'olio del compressore. Occorre tenere presente questo fatto quando si considera il problema della sicurezza.
Già negli anni '30 furono costruiti frigoriferi domestici funzionanti a propano. Le differenze di tipo impiantistico rispetto ai frigoriferi prodotti oggigiorno sono riportate nella seguente tabella:
| 1936 | 1998 |
| Compressore aperto | Compressore ermetico |
| Motore elettrico aperto | Motore nel compressore ermetico |
| Valvola d'espansione | Tubo capillare |
| Scambiatore di calore a tubo alettato | Evaporatore tipo roll-bond |
| 250 grammi di propano | 20 grammi di isobutano |
L'utilizzo degli idrocarburi presenta molti vantaggi, ma anche svantaggi legati alla loro infiammabilità e alla necessità di definire standard di elevata sicurezza, soprattutto quando vengono impiegati in larga quantità.
L'ammoniaca: un refrigerante vecchio e nuovo
L'ammoniaca è uno dei primi refrigeranti utilizzati con successo in un ciclo a compressione di vapore. Anche quando i CFC ottennero un vasto impiego, l'ammoniaca continuò ad essere utilizzata in alcuni impianti speciali in tutto il mondo.
A riguardo dell'ammoniaca è disponibile una notevole esperienza tecnologica. Ciò può essere vantaggiosamente sfruttato in altri impianti dove, ad esempio, l'R22 è largamente utilizzato. A confronto con l'R22 e l'R502 l'ammoniaca presenta alcuni vantaggi:
- Minor costo
- Miglior efficienza nel ciclo frigorifero per diversi valori di temperatura
- Coefficienti di trasferimento del calore migliori
- Temperatura critica più elevata
- Facilità nell'individuazione delle fughe
- Minor costo di pompaggio negli impianti con ricircolo del liquido
- Grande tolleranza in occasione di contaminazione con acqua
- Nessun effetto sullo strato d'Ozono o sul riscaldamento globale
- Minor dimensione delle tubazioni per ottenere la medesima capacità frigorifera
- Problema di solubilità con l'olio
- Incompatibilità con vari tipi di materiali
- Elevate temperature di mandata
Utilizzo dell'acqua come refrigerante
Negli impianti ad assorbimento l'acqua viene utilizzata come refrigerante già da tempo. Essa viene utilizzata anche in cicli a compressione anche in impianti di nuova concezione. L'intero impianto lavora ad una pressione molto inferiore a quelle cui siamo normalmente abituati. La differenza tra la pressione di condensazione e quella di evaporazione è ridotta, ma il rapporto di compressione è molto elevato. Questo significa che per la sua compressione sono necessari compressori centrifughi e che il processo di compressione deve avvenire in più stadi.
Utilizzo dell'anidride carbonica come refrigerante
L'utilizzo dell'anidride carbonica come fluido frigorifero negli impianti di refrigerazione e a pompa di calore riscuote sempre più interesse nell'ottica della sostituzione dei CFC. Essa costituisce una valida alternativa, sia dal punto di vista ecologico che economico, all'utilizzo dei refrigeranti HFC.
Le proprietà e le caratteristiche termofisiche dell'anidride carbonica sono abbastanza diverse da quelle dei tradizionali refrigeranti utilizzati nei cicli a compressione di vapore. Il suo utilizzo, tuttavia, è limitato dai valori critici della sua temperatura (31,1°C) e della sua pressione (73,8 bar).
Un più proficuo utilizzo delle sue proprietà termofisiche può essere raggiunto attraverso la conduzione di cicli trascritti. Essi rappresentano una promettente possibilità sia dal punto di vista ecologico che dal punto di vista della sicurezza. Processi trascritti dell'anidride carbonica possono essere vantaggiosamente utilizzati in impianti per il condizionamento, per il riscaldamento, per il recupero del calore, e nella tecnologia dell'essiccazione.
L'utilizzo della CO come fluido refrigerante garantisce la possibilità di operare in sicurezza e di avere buone prestazioni.
A tutt'oggi permangono differenti punti di vista nelle varie nazioni a riguardo dei potenziali rischi connessi alle scelte dei possibili sostituti dei CFC. Non è indispensabile prendere una decisione che privilegi una via piuttosto che un'altra. Infatti è possibile intraprendere contemporaneamente strade diverse con l'obbiettivo di minimizzare l'impatto sull'ambiente sempre ponendo attenzione sui potenziali rischi nei riguardi dell'umanità.
Idrocarburi Policiclici Aromatici (IPA)
L'inquinamento atmosferico interessa principalmente i grandi centri urbani e gli abitati prossimi ai complessi industriali. Nell'atmosfera di una città quotidianamente s'immettono tonnellate di anidride solforosa, di polveri in sospensione, di idrocarburi, di ossidi di azoto. Nella tabella 1 sono riportati, i principali inquinanti atmosferici:
| Inquinanti | Principali fonti antropogeniche | Emissioni antropogeniche sul totale per anno (milioni di tonnellate) | Tempo medio di permanenza nell'atmosfera |
|---|---|---|---|
| Monossido di carbonio | Uso di combustibili fossili, combustione di biomasse | 700/2000 | mesi |
| Anidride Carbonica | Uso di combustibili fossili, deforestazione | 5000/5500 | 100 anni |
| Metano | Discariche, produzione di combustibili | 300/550 | 100 anni |
| Ossidi di azoto | Uso di combustibili fossili | 20/50 | giorni |
| Idrocarburi policiclici aromatici | Combustioni | 10/20 | mesi |
| Biossido di zolfo | Uso di combustibili fossili, fonderie | 100/200 | da giorni a settimane |
Origine e concentrazioni dei più importanti inquinanti presenti nell'atmosfera
La natura chimica e lo stato fisico, sotto il quale si ritrovano presenti nell'atmosfera, sono due caratteristiche importantissime degli inquinanti atmosferici, in quanto determinano sia il tipo sia l'entità degli effetti, che i contaminanti svolgono all'interno dell'organismo umano.È questo il motivo per cui abbiamo riposto la nostra attenzione su una particolare classe di molecole inquinanti: gli idrocarburi policiclici aromatici (IPA).
Gli IPA sono ritenuti tra i maggiori responsabili della comparsa di danni alla salute delle popolazioni; inoltre le loro caratteristiche chimico-fisiche fanno sì che, pur essendo usualmente emessi nell'atmosfera sotto forma gassosa, tendano rapidamente a condensarsi. Tale caratteristica facilita l'adsorbimento sulla superficie del particolato, per questo il motivo nella nostra ricerca ci siamo occupati anche del particolato atmosferico.
Riguardo alla potenzialità di danno degli IPA, vari studi hanno dimostrato che l'esposizione ad elevate concentrazioni provoca un aumento dell'incidenza di patologie tumorali ai polmoni, alla pelle e ad altre zone esposte a questi composti.
Il potenziale effetto cancerogeno differisce tra le vari molecole e per alcune di queste non è stata ancora determinata l'effettiva capacità di danno. L'Agenzia per la Ricerca sul Cancro (IARC) ha classificato, fino ad ora, 48 IPA in funzione della loro capacità di fungere da induttori tumorali; di questi riportiamo la classificazione dei composti che più frequentemente si ritrovano nell'aria:
| Nome | Grado di cancerogenicità (IARC)1 |
|---|---|
| Benzo(a) pirene | 2A |
| Benzo(a) antracene | 2A |
| Dibenzo(ah) antracene | 2A |
| Benzo(b) fluorantene | 2B |
| 5-metil-crisene | 2B |
| Dibenzo(a,h) acridine | 2B |
| Dibenzo(a,i) pirene | 2B |
| Benzo(ghi) penlene | 3 |
| Metilfemantrene | 3 |
| Crisene | 3 |
| Antracene | 3 |
| Fluorene | 3 |
Classificazione dei principali IPA e loro cancerogenicità 1 2A: Probabilmente cancerogeno per l'uomo; 2B: possibile cancerogeno sull'uomo; 3: Non classificabile come cancerogeno per l'uomo.
Struttura e nomenclaturaGli idrocarburi ad anelli benzenici condensati rappresentano una vasta classe di molecole aromatiche, essi sono costituiti dalla fusione di due o più anelli benzenici, gli anelli vicini sono uniti fra loro tramite una coppia di atomi di carbonio condivisi. I termini più rappresentativi sono riportati nella figura seguente:

Idrocarburi aromatici ad anelli benzenici condensati
Possiamo notare come l'antracene e il fenantrene siano due isomeri; nel primo i tre anelli benzenici sono fusi in maniera lineare, nel secondo in maniera angolare.Teoricamente il numero di IPA è enorme; per esempio, l'unione di cinque anelli benzenici, nelle varie combinazioni, può dare origine a ventidue composti diversi. È possibile ottenere 88, 333 e 1448 composti, utilizzando rispettivamente sei, sette e otto anelli.
La nomenclatura IUPAC attribuisce un numero progressivo agli atomi di carbonio, capaci di legare un sostituente e una lettera minuscola (a-b-c ecc.) unita al numero dell'atomo di carbonio immediatamente precedente, a quelli che costituiscono una giunzione tra due anelli:
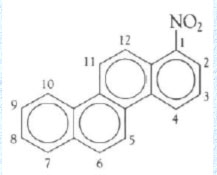
1-Nitropirene
Inoltre, si conoscono molti idrocarburi polibenzenoidi che vengono denominati benzo-derivati, nei quali la posizione di fusione è identificata da una lettera tra parentesi quadra, che indica su quale lato del sistema genitore è avvenuta la fusione: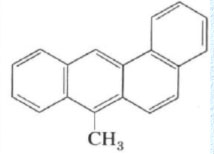
7-Metilbenz[a]antracene
Proprietà chimico, fisiche e reattivitàCome tutti i composti aromatici, anche gli IPA, presentano proprietà simil-benzeniche: stabilità elevata, struttura geometrica piana.
Le proprietà chimiche e fisiche dipendono dalle loro dimensioni (numero di atomi di carbonio) e dalla struttura del sistema di elettroni p. Gli IPA sono solidi a temperatura ambiente e hanno punti di ebollizione e di fusione elevati.(1) Tali composti sono altamente lipofili e sono generalmente insolubili in acqua.
A causa dell'alta lipofilia, gli IPA tendono ad associarsi con le sostanze particellari o con le sostanze oleose presenti nei sistemi acquosi. La solubilità in acqua decresce all'aumentare del peso molecolare, per cui gli IPA con più di quattro anelli si trovano sempre legati alle sostanze particellari, mentre gli IPA a basso peso molecolare (due o tre anelli) possono anche trovarsi liberi nei sistemi acquosi.
La tensione di vapore di questo composti è bassa ed è inversamente proporzionale al numero di anelli contenuti. Per questo motivo spesso gli IPA nell'atmosfera si associano con il articolato aereo. Inoltre si può osservare come al diminuire della temperatura, gli IPA aventi peso molecolare più elevato (³ 4 anelli), caratterizzati da una bassa tensione di vapore, tendano rapidamente a condensare e a venire adsorbiti alla superficie delle particelle di fuliggine e di cenere, mentre quelli a minore peso molecolare (3 anelli), aventi un'alta tensione di vapore, rimangono parzialmente nella fase di vapore per poi condensare. Quindi in un campione di aria gli IPA ad elevato peso molecolare si trovano esclusivamente legati al particolato, mentre quelli a basso peso molecolare possono anche trovarsi liberi nell'atmosfera.
Sono stati misurati i rapporti tra le concentrazioni degli IPA, presenti sotto forma di particelle condensate, e quelle degli stessi composti in fase gassosa, in questo modo è stato possibile evidenziare la distribuzione dei composti analizzati.
Gli idrocarburi policiclici aromatici subiscono facilmente reazioni di sostituzione piuttosto che di addizione sull'anello. Questo avviene perché le reazioni di sostituzione non distruggono la nuvola di elettroni π delocalizzati, nuvola che contribuisce alla stabilità della molecola.
La reattività chimica degli IPA è influenzata da molti fattori ambientali fra i quali la temperatura, la luce, i livelli di ossigeno e di ozono, la presenza di co-inquinanti e di materiale capace di adsorbirli.
È stato osservato che la reattività degli IPA puri è maggiore rispetto a quella riscontrata negli idrocarburi adsorbiti su fuliggine, ciò suggerisce che l'adsorbimento su materiale particolato funga da protezione nei riguardi della foto-ossidazione. L'ossidazione fotochimica è uno fra i più importanti processi di decomposizione degli IPA.
In genere, gli idrocarburi policiclici aromatici mostrano due bande di assorbimento nella regione dell'ultravioletto, la prima cade a circa 200 nm, ed è la più intensa, la seconda si trova a lunghezze d'onda più alte, intorno a 260 nm, è risulta sempre più debole. Se nell'anello vengono introdotti dei gruppi in grado di estendere la delocalizzazione del sistema di elettroni p, entrambe le bande si spostano verso lunghezze d'onda più alte. Un analogo spostamento si osserva nei composti policiclici in cui gli anelli benzenici sono fusi linearmente tra loro.

Gli IPA possono subire anche ossidazioni chimiche reagendo con i radicali liberi e con l'ozono. Queste reazioni non sono influenzate dalla luce. La reazione con l'ozono dipende solo dalla struttura degli IPA. Altri studi hanno dimostrato come alcuni IPA si ossidano rapidamente al buio solo se sono adsorbiti su particelle contenenti radicali liberi.
Gli IPA possono reagire con NO2, SO2 e SO3 se sono esposti alla luce e in presenza di acido solforico e nitrico.
Composti policiclici aromatici con anelli benzenici fusi linearmente
Meccanismo di formazione degli IPAGli IPA si formano in seguito a processi di combustione incompleta di materiali organici contenenti carbonio. Il meccanismo è alquanto complesso: si ha una ripolimerizzazione, in carenza di ossigeno, dei frammenti di idrocarburo che si formano durante il processo di cracking, termine con cui è indicato il processo di demolizione delle frazioni più altobollenti, ricavate dalla distillazione del petrolio, in frazioni più volatili. Durante questo processo le molecole si spezzano e si riarrangiano in molecole più piccole. In generale, dopo i processi di cracking e di combustione, si nota il prevalere dei frammenti contenenti due soli atomi di carbonio. Questi radicali liberi a due atomi di carbonio reagiscono con una molecola di acetilene, C2H2.
Il risultato di tale reazione è un altro radicale a quattro atomi di carbonio:
Il radicale che si forma in questa reazione può in seguito addizionare un'altra molecola di acetilene e formare un anello a sei atomi di carbonio:
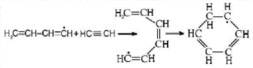
A questo punto l'atomo di idrogeno, legato al carbonio del CH2, può staccarsi dando origine a una molecola di benzene oppure può addizionare altre molecole di acetilene dando luogo a catene laterali che formano ulteriori anelli benzenici condensati:
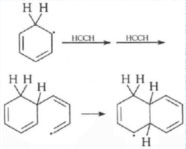
Le temperature elevate (650-900 °C) e la carenza di ossigeno favoriscono la formazione degli IPA; infatti, generalmente, col diminuire del rapporto ossigeno-combustibile si ha un incremento della velocità della loro formazione.
Origine degli IPA
Gli IPA fra i comuni inquinanti ambientali sono una delle classi più pericolose; le principali fonti sono rappresentate dal traffico autoveicolare (emissioni dagli scarichi dei motori a diesel e a benzina), dai processi industriali, dal catrame, dal fumo esalato durante la combustione incompleta del carbone o del legno, e in misura minore dal fumo delle sigarette e dalla superficie di alimenti affumicati; a queste sorgenti artificiali bisogna, poi, aggiungere le fonti naturali rappresentate dalle eruzioni vulcaniche e dagli incendi delle foreste.
Le polveri dell'ambiente urbano sono composte da vari tipi di fuliggine, che vengono emessi essenzialmente dai veicoli a motore. Questa fuliggine contiene quantità variabili di composti genotossici attivi altamente adsorbiti fra i quali, oltre agli idrocarburi policiclici aromatici, si trovano anche i loro nitroderivati (fra i quali il nitropirene e il dinitropirene) e i nitroareni, particolarmente abbondanti nel particolato ultrafine (<1.1 mm) dei motori diesel; spesso questi composti sono risultati cancerogeni più attivi dei corrispondenti idrocarburi non sostituiti. Per questo motivo le emissioni diesel sono state considerate come probabili agenti cancerogeni per l'uomo dall'Agenzia Internazionale per la Ricerca sul Cancro.
Questi composti possono essere inalati in quantità notevoli dall'uomo in certe attività lavorative: asfaltatura di strade, impermeabilizzazioni edilizie mediante catramatura a caldo, conduzione di forni a carbone; inoltre è stato evidenziato un possibile rischio per coloro che lavorano in zone ad elevato traffico autoveicolare, come i vigili urbani e gli addetti ai servizi di pulizia delle strade del centro.
L'esposizione professionale a sostanze contenenti questi idrocarburi causa un aumento dell'incidenza di varie patologie fra cui il carcinoma polmonare e gli epiteliomi cutanei. Sono numerose le sperimentazioni che hanno dimostrato come il contatto cutaneo ripetuto produce epiteliomi in tutte le specie animali. Neoplasie attribuibili a questi idrocarburi sono state osservate, anche di recente, soprattutto nei lavoratori del catrame esposti per via inalatoria o per contatto cutaneo. In passato sono state descritte casistiche di neoplasie polmonari nei soggetti addetti alla produzione del gas dal carbone fossile e di tumori cutanei nei soggetti esposti a oli minerali.
Poiché gli IPA sono potenti cancerogeni nella sede di contatto, per molti anni sono stati classificati tra i cancerogeni ad azione diretta; ricerche più recenti sembrano indicare che anche per queste molecole il vero composto attivo sia un derivato metabolico in forma di epossido.
Purtroppo, oggi gli IPA rischiano di contaminare in modo irreparabile tutte le matrici ambientali, infatti, in seguito alla fuoriuscita del petrolio dalle navi-cisterna, dalle raffinerie e dai punti di trivellazione, si sono rinvenute tracce di questi inquinanti anche nelle acque (mari, fiumi, falde acquifere) e nel suolo, oltre che naturalmente nell'aria. Inoltre, sempre più spesso si osservano fenomeni di bio-accumulo, poiché gli IPA a più alto peso molecolare tendono ad accumularsi nei tessuti adiposi di alcuni organismi marini e questo spiega l'aumento dell'insorgenza di lesioni e tumori epatici in alcuni pesci.
Gli IPA sono contenuti anche nel fumo da tabacco, caratterizzato da una costituzione chimica complessa. Numerose ricerche sono state eseguite per accertare la pericolosità di tali sostanze nei confronti delle persone che fumano e di quelle che vi si trovano esposte (inquinamento indoor).
L'importanza della prevenzione
Per migliorare la qualità dell'aria e ridurre lo sviluppo dello smog fotochimico, ora che è chiara la sua pericolosità, una delle strade che non possono essere escluse è quella della prevenzione.
Occorre ridurre l'emissione dei reagenti responsabili del processo, in primo luogo NOx, idrocarburi contenenti legami C=C e più in generale tutti i COV.
Un tentativo è già stato effettuato in parecchie aree "a rischio" in tutto il mondo, cercando di limitare le emissioni di idrocarburi: il risultato è stata sì una diminuzione percentuale di questi reattivi, ma ciò non è avvenuto ugualmente per gli altri. Questo accade perché sono gli ossidi d'azoto e non gli idrocarburi a determinare la velocità delle reazioni del ciclo fotolitico, quindi la riduzione delle emissioni riesce solo ad abbassare le concentrazioni di questi ultimi, non a diminuire l'entità dello smog. Ciò è dovuto anche alla grande quantità di reazioni che portano alla formazione dello smog, che rendono difficile stabilire quali diminuzioni di reagenti sono realmente utili ai fini della sua riduzione.
Come già detto, gli idrocarburi con legami C=C sono il tipo di sostanza pi� reattiva nei processi di formazione dello smog, ma l'insieme dei responsabili si allarga all'aumentare dei radicali liberi. Questo comporta, nelle aree con seri problemi di inquinamento fotolitico, la necessità di monitorare le emissioni di tutti i tipi di COV.
Le benzine ad esempio, una complessa miscela di idrocarburi, oggi vengono studiate e prodotte con l'obiettivo di ridurne l'evaporazione, che contribuiscono in modo significativo alla concentrazione dei composti organici nell'atmosfera.
Purtroppo però la quantità di autoveicoli in circolazione rende questa misura quasi irrilevante, cerchiamo di capire perché, analizzando il processo di combustione che avviene nei veicoli a motore e le contromisure già attuate.
Nel corso degli ultimi 15 anni si è cercato di attuare un controllo completo sulle emissioni di NOx provenienti dagli autoveicoli con l'utilizzo di convertitori catalitici montati dopo la marmitta (meglio noti come marmitte catalitiche). Gli originali convertitori a due vie sono attivi solo sui gas a base di carbonio, come il monossido di carbonio CO, completandone la combustione fino al prodotto ultimo, il biossido di carbonio.
I più recenti convertitori a tre vie invece utilizzano una superficie impregnata di catalizzatore a base di Rodio per trasformare prima gli ossidi di azoto in azoto e ossigeno elementare utilizzando idrocarburi incombusti, CO e H2, come agenti riducenti.
2 NO ——» N2 + O2
Quindi con un catalizzatore a base di platino e/o palladio i gas contenenti carbonio sono quasi tutti ossidati a CO2 e acqua.
2 CO + O2 ——» 2 CO2
Infine è prevista la presenza di una sonda sensibile all'ossigeno, che mantenga un elevato livello di conversione degli inquinanti intervenendo sul rapporto aria/combustibile.
Il convertitore a tre vie, una volta raggiunta la temperatura operativa, elimina l'80/90% degli idrocarburi/CO/NOx presenti negli scarichi del motore.
Tuttavia, soprattutto in città dove l'andatura è spesso incostante, il catalizzatore non opera sempre efficientemente in presenza di improvvise accelerazioni o decelerazioni determinando picchi di emissioni inquinanti.
Di fondamentale importanza è anche la perfetta manutenzione del catalizzatore: è stato studiato e stabilito che una marmitta catalitica danneggiata (basta un rifornimento di benzina con piombo) emette la maggior percentuale di inquinanti: il 50% delle emissioni di CO infatti è dovuto al solo 10% di veicoli. Da qui la necessità di continui ed accurati controlli ai sistemi di scarico, spesso sottovalutati ma di estrema importanza.
La prevenzione a Modena
La nostra provincia già da anni ha avviato programmi di ricerca ed informazione sui rischi e la prevenzione derivati dallo smog per sensibilizzare tutti i cittadini a questo grave problema. Normative ambientali e leggi sanitarie sono già in vigore al fine di ridurre l'impatto degli insediamenti produttivi sulla qualità dell'aria e delle acque.
Le linee operative di queste norme si basano anzitutto sulla prevenzione, materie prime e cicli tecnologico-produttivi sono quindi tra gli obiettivi principali.
Già dal 1990 sono in vigore limiti di emissione nell'atmosfera per tutti gli inquinanti, in funzione della loro tossicità; in seguito le spese per portare i propri impianti "a norma" hanno spinto le aziende alla sostituzione delle materie prime più nocive con altre di minore impatto ambientale, alla modificazione dei cicli produttivi, all'installazione di sistemi di depurazione.
Esistono anche certificazioni di qualità, assegnate alle aziende che autonomamente e al di là delle richieste legislative cercano strade ancora nuove per migliorare ulteriormente i propri standard di salubrità sul lavoro.
| Inquinante | Valore Limite (μg/m3) | riodo di Mediazione | Nr. Max di superamenti l'anno |
| Biossido di Zolfo | 125/350 | 24h/1h | 3/24 |
| Biossido di Azoto | 40/200 | 365gg/1h | -/18 |
| Monossido di Carbonio | 10 | Media max giornaliera su 8 h | - |
| Polveri Sottili | 40/50 | 365 gg/24 h | -/35 |
| Benzene | 5 | 365 gg | - |
| Piombo | 0,5 | 365 gg | - |
| Ozono | 180 | 1h | - |
Occorre tuttavia sottolineare la presenza di stabilimenti che a causa delle dimensioni o delle peculiarità produttive vedono risultare inattuabile un'azione di sostituzione delle proprie materie prime, rendendo obbligata la scelta degli impianti di depurazione.
Esempio ideale sono i processi di verniciatura in genere, responsabili di consistenti emissioni di COV: dovendo garantire particolari qualità ai propri prodotti, le aziende per adeguarsi alla normativa hanno installato appositi sistemi di depurazione; tra questi ricordiamo il combustore termico, un sistema che attraverso il passaggio del flusso inquinato all'interno di una camera di combustione mantenuta ad elevata temperatura, provoca l'ossidazione delle sostanze organiche e garantisce elevata efficienza di depurazione.
Col tempo però è stato considerato che i costi di smaltimento via combustione, per alcuni flussi, diventavano improponibili. La soluzione è stata trovata nel 1998, adottando una tecnica che negli USA e nel resto d'Europa era già in uso dai primi anni 90 soprattutto tra le imprese dei settori automobilistico e dei semiconduttori: il sistema rotore concentratore a zeoliti.
L'apparato in questione sfrutta le zeoliti inorganiche idrofobe (materiali di sintesi a base di silicio) e la loro grande capacità adsorbente nei confronti dei COV in qualsiasi condizione, anche con alte % di umidità o temperature molto elevate.
L'impianto, sinteticamente, è costituito da un rotore strutturato a nido d'ape a base di fibre di vetro impregnate di grani di zeoliti idrofobe di 2 micron circa.
La velocità del rotore è determinata in base al carico inquinante da trattare, tale da consentire simultaneamente, in zone diverse, i processi di adsorbimento e desorbimento ad alta temperatura, con successivo invio alla depurazione tramite combustione.
Dopo l'installazione di questi nuovi impianti sono state svolte opportune analisi dalla provincia per verificare la loro effettiva efficacia: l'adsorbimento del flusso inquinante avviene a T ambiente con una resa di abbattimento del 95% e scarico diretto in atmosfera.
Il desorbimento avviene praticamente su una frazione del flusso in uscita dal rotore, questo viene riscaldato a 180°C e, dopo essere stato privato del solvente subisce una altro ciclo di adsorbimento da parte degli zeoliti.
Il flusso quindi, concentrato, viene indirizzato all'ossidazione termica (97% di resa) che infine scarica in atmosfera un prodotto più che accettabile.
Successive rilevazioni ambientali hanno provato che l'impiego dei nuovi impianti ha ridotto del 94% il carico giornaliero di sostanze organiche emesse in atmosfera.
Gli eccellenti risultati però non devono far dimenticare che la depurazione è pur sempre da considerarsi l'ultima strada da percorrere, anche se impianti come questo testimoniano che lo sviluppo nel rispetto dell'ambiente è possibile.
Effetti dell'inquinamento aereo sulla salute
Intuitivamente è lecito aspettarsi che i maggiori danni subiti dal nostro organismo causa elevata esposizione ad aria inquinata si abbiano a livello dei polmoni.
In soggetti già sofferenti di patologie all'apparato respiratorio in effetti, come gli asmatici, i problemi di insufficienza respiratoria aumentano vertiginosamente quando nell'aria che respirano si denota un aumento dei livelli di SO2 e O3.
In generale, per qualsiasi individuo, i più gravi problemi respiratori sono causati da particolati di SO2 e fuliggine; ne sono prova i numerosi episodi, negli anni '50, di aumenti vertiginosi dei tassi di mortalità in corrispondenza di smog a base di zolfo e fuliggine. In Inghilterra nel 1952 circa 4000 persone morirono in un solo mese a causa dello stagnare a livello del suolo di una massa nebbiosa contente i suddetti inquinanti.
I più esposti a questo tipo di rischi oltre alle persone già sofferenti di problemi respiratori si sono rivelati gli anziani ed i bambini; questo problema è stato praticamente risolto bandendo dalle case i principali responsabili, i sistemi di riscaldamento a carbone, anche se non è stato ancora stabilito se gli effettivi responsabili fossero SO2, goccioline o particolati di H2SO4.
Oggi fortunatamente grazie ai sistemi di controllo di nebbie acide e fuliggini le morti per bronchiti sono calate del 50% nel Europa occidentale, mentre ad Est la situazione è ancora critica a causa dello sfruttamento massiccio di lignite ad alto tenore di zolfo per combustione. Nello stesso occidente pur avendo eliminato lo smog chimico a base di zolfo i problemi non sono finiti: molti abitanti di questi paesi ancora oggi si trovano cronicamente esposti a livelli misurabili di acido solforico e solfati a causa del trasporto a lunga distanza dalle regioni industrializzate che continuano a produrre SO2. Contemporaneamente esistono prove reali che l'acidità dell'inquinamento sia il principale responsabile di disfunzioni polmonari, compresi i problemi respiratori e le bronchiti dei bambini.
Recentemente si è anche ipotizzato che l'inquinamento da SO2 e solfati diminuisca la resistenza dell'organismo al cancro del colon e della mammella. L'ipotesi è sostenuta da una teoria secondo la quale il biossido di zolfo assorbirebbe ingenti quantità di una radiazione detta UV-B; questa radiazione è essenziale per la biosintesi della vitamina D, un agente protettivo per i tipi di cancro sopraelencati, e considerando che i solfati le disperdono questo tipo di inquinamento riduce di molto la quantità di radiazione che raggiunge il suolo.
L'ozono, ad insaputa di molti, è un inquinante tossico dell'aria. La sua famosa funzione protettiva nei confronti dei raggi U.V. infatti è tale solo nelle parti più alte della nostra atmosfera, dove l'aria è molto più rarefatta. A differenza dello zolfo, l'O3 causa effetti eguali sia su persone sane che affette da disturbi respiratori, cioè irritazioni nel naso e nella gola, tosse, fino ad arrivare a veri e propri dolori toracici dopo un respiro profondo.
Tali effetti infatti si riscontrano spesso in persone in perfetta salute, come gli atleti, che si allenano o gareggiano in episodi di smog. Si è riscontrato che i tempi delle prestazioni di sportivi si alzano proporzionalmente al livello di smog dell'aria che respirano.
A causa della ripetuta esposizione a questi inquinanti l'organismo si trova a far fronte ad una progressiva distruzione del tessuto polmonare, facilitando l'insorgere di malattie infettive.
Va però ricordato che in gran parte dell'occidente i danni da smog fuligginoso sono stati arginati efficacemente già da alcuni anni; il parametro che ora fornisce indicazioni riguardo la mortalità è dato dalla concentrazione dei particolati.
Grafici del tasso di mortalità giornaliero in funzione dei valori di PM10 del giorno stesso o precedente mostrano una notevole linearità; in funzione di queste ricerche è stato stimato che un aumento di 100 μg/m³ dell'indice PM10 determina un aumento della mortalità del 6/17%.
Va infine ricordato che spesso i limiti di emissione fissati non sono sufficienti a garantire una completa sicurezza dai problemi di salute, ma è ancora più preoccupante il fatto che per la maggior parte dell'anno solare questi limiti vengono ampiamente superati.
Rete di centraline della provincia di Modena
| Stazione | Tipologia dell'Area | Parametri monitorati |
|---|---|---|
| MO-Garibaldi | Urbana/Traffico intenso | SO2, NOx, CO, O3, PTS |
| MO-Giardini | Urbana/Traffico intenso | NOx, CO, PTS |
| MO-Cavour | Urbana | NOx, CO, meteo |
| MO-Nonantolana | Urbana/Tangenziale | NOx, CO, O3, PTS, PM10, BTX |
| MO-XX Settembre | Urbana/Zona a traffico limitato | NOx, CO, O3, PTS, PM10, BTX |
| Campogalliano | Urbana/Strade ad alto traffico | NOx, CO |
| Carpi 1 | Urbana/Traffico intenso | NOx, CO, PTS |
| Carpi 2 | Urbana/Zona a traffico limitato | NOx, CO, PM10, BTX, meteo |
| Castelfranco | Urbana/Strade ad alto traffico | NOx, CO |
| Mirandola | Urbana/Traffico intenso | NOx, CO, O3, meteo |
| Pavullo | Urbana/Strade ad alto traffico | SO2, NOx, PTS |
| Sassuolo | Urbana/Strade ad alto traffico | NOx, CO, PTS, BTX |
| Spezzano 1 | Rurale | O3, PTS, meteo |
| Spezzano 2 | Urbana | NOx, CO |
| Maranello | Urbana | NOx, CO, O3, BTX |
| Solignano | Industriale in prossimità zona rurale | PTS, meteo |
| Staz.Rilocabile SAT | Urbana/Traffico/Industriale | NOx, CO, O3, PM10, meteo |
Metodi chimici d'analisi
Spettrofotometria UV
La spettrometria UV si basa sull'assorbimento selettivo, da parte di molecole (eventualmente ionizzate), delle radiazioni di lunghezza d'onda comprese tra 10 e 780 nm. Quest'ampia gamma spettrale è suddivisa in tre regioni principali: UV lontano, UV vicino e visibile. Dal punto di vista analitico le regioni più utilizzate sono l'UV vicino e visibile. Viene eseguito uno spettro del campione in esame con luce UV irradiata a lunghezze d'onda variabili e con continuità. Le radiazioni assorbite corrispondono in termini di energia alle quantità necessarie ad aumentare i livelli energetici degli elettroni p. L'identificazione dell'analita avviene mediante lo studio dello spettro la cui struttura dipende dal sistema coniugato di elettroni presenti nella molecola.
Chemioluminescenza
La luminescenza consiste fondamentalmente nell'emissione di radiazioni luminose nel visibile o nel vicino visibile (lunghezza d'onda compresa nell'intervallo 300-800 nm) dopo che elettroni eccitati mediante una fonte di energia, ritornano dallo stato eccitato a quello fondamentale. L'energia potenziale delle transizioni elettroniche all'interno degli atomi o delle molecole viene così liberata sotto forma di luce.
Spettroscopia IR
La spettroscopia infrarossa è una tecnica che si basa sull'interazione delle molecole con l'energia della radiazione infrarossa. Un composto organico irradiato dalla radiazione elettromagnetica assorbe a una determinata lunghezza d'onda e si lascia attraversare dalle altre. Irradiando il composto con numerose lunghezze d'onda si può ottenere un grafico chiamato "Spettro di Assorbimento". L'interpretazione completa di uno spettro IR è un operazione piuttosto difficile, poiché occorre determinare la natura di ognuno dei picchi di stretching (stiramento) e bending (piegamento) riferiti agli effetti della radiazione assorbita sulla molecola. Identificando la maggiorparte di questi picchi caratteristici risulta quasi sempre possibile risalire alla natura del campione analizzato.
Gascromatografia
La tecnica si basa sulla differente affinità che i diversi componenti del campione manifestano nei confronti della fase mobile (un gas permanente) che fluisce attraverso la colonna in cui è posta la fase stazionaria. All'uscita della colonna un rivelatore segnala il passaggio dei diversi componenti della miscela a un sistema di elaborazione dei segnali. Il tracciato gascromatografico che si ottiene consente di risalire alle quantit� relative delle diverse sostanze e in molti casi, con opportuni accorgimenti, alla loro natura chimica.
Spettrofotometria di massa
In uno spettrometro di massa una molecola organica viene ionizzata, nel caso più comune per interazione con un fascio di elettroni con energia di circa 75 eV.
Lo ione molecolare carico positivamente si frammenta (in parte), con formazione di molecole e/o radicali neutri, che non vengono rivelati dallo strumento, e di cationi e/o radicali cationi, separati e rivelati dallo spettrometro.
In uno spettro di massa, l'asse delle x riporta valori di rapporto massa/carica e l'asse delle y valori di abbondanza relativa degli ioni analizzati.
Dallo spettro di massa si può risalire alla struttura di un composto incognito attribuendo una composizione elementare (e possibilmente una formula di struttura) ai singoli ioni e ricostruendo i meccanismi di frammentazione seguendo schemi tipici per le varie classi di composti.
Lo spettrometro di massa può essere direttamente interfacciato ad un gas-cromatografo o ad un cromatografo liquido ad alta efficienza; miscele complesse di prodotti possono quindi essere risolte nei singoli componenti ed i singoli spettri possono essere interpretati o confrontati con librerie standard di spettri di composti noti.
Spettrofotometria in Assorbimento Atomico
La spettrofotometria di assorbimento atomico è una delle tecniche più usate oggi per l'analisi degli elementi in tracce (soprattutto metalli) in matrici di ogni genere: da quelle ambientali, come aria, acque e terreni, fino agli alimenti e leghe metalliche.
Questa tecnica si presta ad analisi di tipo sia qualitativo che quantitativo degli elementi, ma di fatto usata quasi esclusivamente per quella quantitativa. In pratica, l'elemento in esame viene atomizzato e bersagliato con radiazioni di lunghezza d'onda opportuna, per effetto dell'assorbimento atomico, l'intensità del raggio diminuisce e l'attenuazione può essere correlata alla concentrazione dell'elemento nel campione mediante una legge analoga a quella di Beer, A = xbN.
Per quanto riguarda gli elementi determinabili, i limiti sono essenzialmente strumentali e derivano dall'assorbimento dell'ossigeno dell'aria e, soprattutto, dal fatto che, con il sistema di atomizzazione a fiamma, i gas caldi assorbono le radiazioni in determinate regioni spettrali.
Ogni elemento ha un determinato n° di elettroni, che lo caratterizza. Poiché nello stato fondamentale gli elettroni occupano gli orbitali disponibili secondo una specifica configurazione (quella di minima energia), l'insieme delle possibili transizioni elettroniche verso orbitali più esterni è caratteristico di ciascun elemento.
Ogni transizione corrisponde all'assorbimento di una precisa energia e produce una riga spettrale con una caratteristica lunghezza d'onda.
Le righe degli spettri di assorbimento ( e di emissione) non sono perfettamente monocromatiche; in realtà si presentano come bande con una ampiezza dell'ordine di 0.002 nm. L'allargamento delle righe spettrali è dovuto a tre fenomeni principali: allargamento do Lorentz, Doppler, Naturale.
Per determinare la quantità di un elemento, si può atomizzare il campione in cui è contenuto, eccitare i suoi atomi con radiazioni di opportuna lunghezza d'onda e misurare la radiazione subita. Alle normali temperature di esercizio la maggior parte degli atomi si trova nello stato fondamentale e una parte, sia pur minima, può trovarsi uno stato termicamente eccitato; questi atomi, perciò, non partecipano al processo di assorbimento che si intende misurare.
L'assorbimento, che dipende dal n° di atomi nello stato fondamentale, è direttamente proporzionale all'intera popolazione di atomi presenti sul cammino ottico della radiazione e quindi alla concentrazione dell'elemento nel campione ( se l'atomizzazione viene ottenuto con una fiamma) oppure alla quantità dell'elemento (se l'atomizzazione viene ottenuta con sistemi senza fiamma).
In queste condizioni l'assorbimento atomico sia pure in un intervallo di linearità abbastanza ristretto segue una legge analoga alla legge di Beer, descritta per l'assorbimento molecolare. Per un generico elemento eccitato da una radiazione monocromatica i cui atomi siano dispersi in fase gassosa:
A = xbN dove x è il coefficiente spettrale di assorbimento atomico b lo spessore dello strato assorbente ( il cammino ottico) N il n° totale di atomi liberi.
Biomonitoraggio
Il monitoraggio dell'inquinamento dell'aria è una delle problematiche più complesse nel campo della salvaguardia ambientale. Nonostante siano presenti molte leggi che prevedono limitazioni sulle concentrazioni degli inquinanti al suolo, la quantità di essi in atmosfera è ancora molto elevata, e probabilmente in alcuni casi è destinata ad aumentare. Una delle principali cause di questo fenomeno è l'incremento demografico e quindi tutte le attività a esso connesse.
Una misura puramente strumentale dell'inquinamento dell'aria non permette di rilevare gli effetti che ha esso sugli ecosistemi.
Il biomonitoraggio invece permette di stimare gli effetti biologici dell'inquinamento. Le tecniche di biomonitoraggio producono dati biologi:
- misure di biodiversità
- misure di variazioni nell'assetto morfologico, fisiologico o genetico degli organismi;
- misure delle concentrazioni di sostanze negli organismi.
Il biomonitoraggio non è alternativo rispetto a quello strumentale, ma è un campo di ricerca autonomo, che può fornire informazioni importanti per il monitoraggio dell'inquinamento, individuando possibili zone a rischio e ottimizzando la localizzazione degli strumenti di misura.
Ci sono diverse tecniche di biomonitoraggio: bioindicazione e bioaccumulo; l'indice di biodiversità lichenica.
Proprio di quest'ultima ci occuperemo in modo più dettagliato.
Caratteristiche generali dei licheni
I licheni sono organismi simbionti composti generalmente da un partner fungino generalmente ascomicete e da un'alga verde.
La simbiosi tra alga e fungo risulta vantaggiosa per entrambi gli organismi: il fungo usufruisce delle sostanze organiche prodotte dalla fotosintesi dell'alga, mentre quest'ultima riceve dal fungo protezione, acqua e sali minerali.
Proprio grazie a questa unione i licheni, i licheni sono in grado di vivere in ambienti diversissimi tra loro, anche quelli caratterizzati da condizioni di vita estreme, dove, da soli, fungo e alga non potrebbero sopravvivere.
La parte esterna del lichene, quella che solitamente si vede sulle cortecce degli alberi, viene definita tallo.
Partendo poi dalla superficie superiore si osservano:
- strato corticale, costituito da cellule fungine caratterizzate da una robusta parete cellulare con pigmentazione gialla, aranciata, grigia o verde;
- strato gonidiale, formato da alghe unicellulari, i gonidi, luogo di attività fotosintetica;
- strato midollare, ottenuto da un fitto intreccio di ife con ampi spazi interposti.
- licheni crostosi: sono caratterizzati da un tallo strettamente aderente al substrato. I talli possono essere continui, areolati (suddivisi in areole piatte), verrucosi (areole convesse), peltati (areole con margini ascendenti attaccate per un punto centrale), leprosi (di aspetto pulverulento costituiti da una massa indifferenziata di ife e alghe), placodiomorfi;

Lichene crostoso del genere calendariella
- licheni squamulosi: sono una variante dei licheni crostosi, il cui tallo è costituito da squamule ascendenti, o da verruche fortemente convesse raggruppate in cuscinetti (talli bullati);
- licheni fogliosi: è costituito da lobi più o meno appiattiti e il tallo è facilmente asportabile, solitamente la loro superficie superiore differisce, per grandezza,da quella inferiore. Le dimensioni dei lobi variano da pochi mm ad alcuni cm;
- licheni fruticosi: il tallo si sviluppa tridimensionalmente, ed è formato da ramificazioni (lacinie) a sezione piatta o circolare. Il portamento può essere eretto oppure pendente, in alcuni casi da un tallo primario crostoso o squamuloso si dipartono delle strutture sub erette, di forma variabile;

Lichene foglioso del genere parmelia
- licheni gelatinosi: sono i licheni crostosi, fogliosi o fruticosi, il cui fotobionte è un cianobatterio, presentano generalmente un colore scuro e una consistenza gelatinosa allo stato umido, mentre appaiono rigidi e fragili in condizioni disidratate.
La moltiplicazione vegetativa avviene tramite frammentazione del tallo, dove l'alga si riproduce attivamente solo per via agamica. La riproduzione sessuata interessa esclusivamente il fungo e avviene tramite la produzione e la dispersione di spore, contenute in strutture sacciformi dette aschi.
Licheni come bioindicatori
I licheni sono molto sensibili agli stress ambientali, specialmente per quanto riguarda l'inquinamento.
I primi studi sui licheni, come possibili bioindicatori risalgono al secolo scorso, ma solo da alcuni decenni sono stati assunti come pratica di biomonitoraggio, grazie alla loro disponibilità di effettuare misure dirette dell'inquinamento, indispensabili per quantificare le relazioni tra concentrazione atmosferica di sostanze dannose e risposta biologica.
Nel biomonitoraggio dell'inquinamento atmosferico, i licheni, permettono di realizzare indagini ambientali complete. Essi infatti possono essere utilizzati sia come bioindicatori (associando determinate quantità di disturbo ambientale a variazione del loro aspetto esteriore) sia come bioaccumulatori (sfruttando la loro capacità di assorbire sostanze dall'esterno).
Le alterazioni indotte dall'inquinamento atmosferico sui licheni, si possono manifestare a tre differenti livelli:
- fisiologico, con generale depressione della fotosintesi e della respirazione cellulare (per danneggiamento della clorofilla, nonché un'evidente riduzione della fertilità);
- morfologico, con evidente scolorimento e modificazione della forma del tallo. In generale avvicinandosi alle sorgenti inquinanti si assiste ad un progressivo peggioramento delle condiziona di salute del lichene;
- ecologico, con generale diminuzione della copertura di specie e alterazioni della comunità lichenica.
I licheni sopravvivono bene a temperature comprese tra meno 20°C e più 70°C, una volta disidratati prove di laboratorio hanno dimostrato che sono in grado di vivere anche a temperature molto drastiche comprese tra meno 196°C e più 100°C.
Nonostante tutto questo, la maggior parte dei licheni, preferisce ambienti caratterizzati da temperature miti ed elevata umidit� atmosferica, tipici delle zone a clima oceanico.
Rilevamento
Per eseguire un rilevamento su una corteccia, secondo il metodo di Nimis del 1999 modificato, abbiamo bisogno di un reticolo di campionamento costituito da quattro sub unità, ciascuna formata da una serie lineare di cinque quadrati di 10x10cm.
La parte inferiore di ciascuna unità deve essere posta all'altezza di un metro dalla superficie del suolo, questa regola può essere leggermente modificata in zone particolarmente aride e in centri urbani, dove spesso la copertura lichenica è ristretta alla base degli alberi, e quindi è permesso andare al disotto di un metro dal suolo; le nostre misure sono state effettuate tutte all'altezza di 1 m dal suolo.
I quattro elementi della griglia vanno posti in corrispondenza dei quattro punti cardinali nord, sud, ovest, est. Anche in questo caso è permesso fare uno strappo alla regola in caso di malformazioni del tronco o zone poco idonee al rilevamento, si può eseguire una rotazione di 20° in senso orario.
Per permettere una ripetizione della rilevazione nella scheda-stazione vanno annotati per ogni albero:
- esatta localizzazione dell'albero, utilizzando un sistema satellitare (GPS);
- altezza dal suolo della base del reticolo;
- esatta posizione di ogni sub unit� di un reticolo.
- Vanno annotate sulla scheda-stazione tutte le specie licheniche presenti, il numero di volte che si presentano, il colore, le dimensioni e possibili danneggiamenti quali decolorazione, necrosi ecc...
GPS
Abbiamo detto che per ripetere l'esperienza dobbiamo conoscere con precisione il luogo in cui andiamo ad effettuare la rilevazione, per questo usiamo un sistema satellitare GPS.
Le stazioni riceventi GPS sono in grado di stimare la propria posizione tridimensionale attraverso un numero ripetuto di misurazioni delle distanze rispetto ad almeno quattro satelliti.
Per ridurre le limitazioni di precisione, che erano state introdotte dal ministero della Difesa dagli Stati Uniti, è stato introdotto il sistema differenziale DGPS, basato sull'utilizzo di un ricevitore addizionale, denominato "stazione base", collocato in una posizione di coordinate note, stabilite con precisione attraverso accurate misurazioni geotopografiche.
Attraverso il sistema DGPS si realizza un significativo miglioramento dell'accuratezza, circa dieci volte maggiore rispetto al normale GPS, ma questo comporta un notevole aggravio dei costi sia per la gestione delle strumentazioni fisse e mobili, che per la necessità di personale qualificato.
Operando in zone sufficientemente aperte, dove sia possibile ricevere i segnali di quattro satelliti, gli errori planimetrici possono essere contenuti entro 25 m, mentre per la determinazione delle quote essendo l'errore superiore di 2-3 volte quello planimetrico, è preferibile far ricorso a buon altimetri tarati con frequenza. Nel nostro caso gli errori planimetrici sono sempre stati inferiori a 10 m, mentre non abbiamo rilevato le altitudini.
Elaborazione dei dati
Il valore di biodiversità lichenica della stazione di campionamento è stimato statisticamente sulla base dei valori rilevati nella stazione stessa.
Il primo passo è sommare le frequenze delle specie rilevate su ciascun albero.
Poiché è prevedibile una sostanziale differenza di crescita sui diversi lati del tronco, le frequenze vanno tenute separate per ciascun punto cardinale.
Per ciascun albero si otterranno quattro somme di frequenze (BLnord, BLsest, BLsud, BLovest).
In ciascuna stazione si effettueranno le seguenti operazioni:
- sommare, per ciascun rilievo, le frequenze di tutte le specie;
- sommare le biodiversità licheniche di tutti i rilievi realizzati nello stesso punto cardinale e dividere per il loro numero;
- sommare le biodiversità dei quattro punti cardinali.


Montaggio del retino in viale Buon Pastore
Biomonitoraggio ambientale a ModenaAbbiamo seguito la metodica della S.L.I. modificata nel 2003, utilizzando stazioni di 3/5 tigli, alberi a corteccia subacida, di dimensioni opportune, (minima circonferenza 60 cm), con un'inclinazione del tronco non maggiore di 10° e privi di evidenti difetti. Il reticolo applicato è formato da una griglia di 5 quadrati di 10x10 cm, applicata ad una altezza di 1m da terra ad ogni punto cardinale.
Abbiamo scelto una trentina di stazioni, dal centro alla periferia, inserendo anche una frazione a sud, Baggiovara e due stazioni nel comparto ceramico. Le uscite di rilevamento sono state effettuate nei mesi di dicembre 2003, febbraio e marzo 2004 e sono tutt'ora in corso. I risultati del calcolo dell'IBL sono stati ottenuti sommando le frequenze licheniche dei singoli punti cardinali dello stesso albero e poi calcolandone la media. Si è calcolata infine la media degli alberi della stazione. In alcuni casi abbiamo potuto prelevare parte del tallo lichenico e a scuola lo abbiamo analizzato al microscopio e con i reattivi KOH, HClO e p-FENILENDIAMMINA, che ci hanno permesso di classificare i licheni tramite la consultazione delle chiavi di classificazione ufficiali.

Stazione di via Piersanti Matarella (centro comm.le Rotonda)
Risultati| Stazione | Localiz. cittadina | Coord. Geografiche | IBL | Qualità dell'aria | Colore |
|---|---|---|---|---|---|
| 1 | Vle. Muratori, ang. largo S. Francesco |
N 44° 38'539 E 10° 55'277 |
9 | Alterazione alta | rosso |
| 2 | V.le N.Fabrizi, dietro teatro Storchi |
N 44° 38'596 E 10° 55'879 |
12 | alterazione alta | rosso |
| 3 | V.le Gramsci dalla Rotonda |
N 44° 39'360 E 10° 55'879 |
27 | alterazione media | arancio |
| 4 | V. Nonantolana dav. Parco 22 aprile |
N 44° 39,198 E 10° 56,265 |
25 | alterazione media | arancio |
| 5 | V. Cervino slargo dav.28-64 |
N 44° 39,452 E 10° 56,845 |
14 | alterazione alta | rosso |
| 6 | V. Emilia ovest dav. Parco Ferrari |
N 44° 39,188 E 10° 54,630 |
14 | alterazione alta | rosso |
| 7 | V. Galaverna dav. Bar e di fronte |
N 44° 39,297 E 10° 54,495 |
25 | alterazione media | arancio |
| 8 | V. Buon Pastore Incrocio C.Sigonio |
N 44° 38,381 E 10° 55,350 |
26 | alterazione media | arancio |
| 9 | V. Buon Pastore incrocio v.le Amendola |
N 44° 38,008 E 10° 55,198 |
10 | alterazione alta | rosso |
| 10 | V. Conco n° civ. 25,44,61 |
N 44° 37,716 E 10° 55,036 |
45 | alterazione bassa | giallo |
| 11 | V. Emilio Po vic. v. Beneventi |
N 44° 38,972 E 10° 53,974 |
34 | alterazione bassa | giallo |
| 12 | V. Nobili/ferrovia La Comm. |
N 44° 39,008 E 10° 53,592 |
36 | alterazione bassa | giallo |
| 13 | V. P.S.Matarella da centro Comm. |
N 44° 37,280 E 10° 55,520 |
54 | naturalità media | verdino |
| 14 | V. C.A.dalla Chiesa parco ciclab.50,52 |
N 44° 37,137 E 10° 55,731 |
52 | naturalità media | verdino |
| 15 | Parco Sc. Rodari dietro fermata bus |
N 44° 37,302 E 10° 56,017 |
53 | naturalità media | verdino |
| 16 | V.Giardini 645 alberi sulla strada |
N 44° 37,969 E 10° 54,082 |
31 | alterazione bassa | giallo |
| 17 | V. Giardini 785 da incrocio v.Panni |
N 44° 37,760 E 10° 53,907 |
29 | alterazione media | arancio |
| 18 | V. Tamburini da incrocio v. Sassi |
N 44° 38,142 E 10° 55,126 |
35 | alterazione bassa | giallo |
Conclusioni
Ci sembra di poter affermare che esiste una buona correlazione (inversa) tra zona ad intenso traffico ed IBL (ovviamente più basso), come mostrano i valori delle prime 9 stazioni monitorate, situate attorno al centro cittadino o in zone di elevatissimo traffico come le stazioni n°16 e n°17. Le stazioni 13, 14 e 15 sono invece situate tutte in zona periferica, vicino ad un centro commerciale costruito 15 anni fa, ma con traffico non elevato la 13, sul retro di una zona residenziale la 14 e vicino ad una scuola con un ampio parco la stazione n°15 . Abbiamo notato nelle zone con qualità peggiore dell'aria anche ridotte dimensioni dei talli lichenici e condizioni di sofferenza interna, o di scarsa pigmentazione: i generi prevalenti Physcia e Physconia, con alcune Lecanore. Nelle stazioni con qualità dell'aria migliore le dimensioni dei talli sono decisamente maggiori, con presenza anche di generi come Xantorie e più esigenti quali le Parmelie.
Abbiamo potuto consultare un unico studio di biomonitoraggio eseguito dall'ARPA di Modena nel 1994, 1997 e 2002, relative a 10 stazioni con specie diverse di alberi (pioppo, olmo, noce), che si estendono dal centro cittadino verso la zona nord-est, dove è situato l'inceneritore. Si evidenzia un progressivo miglioramento della presenza lichenica nel tempo, in relazione alle diminuite emissioni di SO2 dai combustibili utilizzati per il riscaldamento e per i trasporti. Nei prossimi anni vorremmo poter continuare il monitoraggio per riuscire a confermare questa tendenza, pur con alcune necessarie riflessioni: una diminuzione della SO2 non ha portato ad una contemporanea diminuzione di NOx, ancora piuttosto elevati, e soprattutto sono in aumento, dai dati delle centraline ARPA, le polveri sottili, inquinanti la cui correlazione con la crescita lichenica non è stata completamente chiarita. Certo nelle zone "peggiori" sono prevalenti specie "nitrofile", cioè; tolleranti nei confronti degli NOx, quali Physcia o Physconia. Le polveri potrebbero avere invece un effetto eutrofizzante, trasportando sui talli sali di ammonio quaternario.